题目内容
【题目】下列有关水溶液中的平衡相关的问题,请填空
(1)已知常温下,将氯化铝溶液和碳酸钠溶液混合,有白色沉淀产生,写出反应离子方程式________。
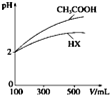
(2)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。同浓度,同体积的CH3COONa与NaX溶液,离子总数目: CH3COONa溶液_______NaX溶液(填>,<,=)
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
①25℃时,浓度均为0.01 mol·L-1 HCN和NaCN混合溶液显_____性(填酸,碱,中)。溶液中HCN浓度_________CN-浓度(填>,<,=)。
②25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中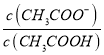 =____________。
=____________。
(4)在25°C下,将x mol·L-1的氨水与y mol·L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH4+)____c(Cl-)(填“>” 、“<” 或“=” );用含x和y的代数式表示出氨水的电离平衡常数______。
【答案】2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑ 小于 > 碱性 > 18 = ![]()
【解析】
(1)氯化铝溶液和碳酸钠溶液混合,发生盐的双水解反应,产生白色氢氧化铝沉淀和二氧化碳气体;
(2)据图分析,加水稀释的过程中,酸HX的pH变化比较慢,说明HX的酸性比醋酸弱;根据电荷守恒分析、比较溶液中离子数目关系;
(3)①比较HCN的电离平衡常数和CN-的水解平衡常数判断溶液的酸碱性;
②结合醋酸的电离平衡常数计算;
(4)根据电荷守恒分析比较离子浓度关系,结合弱电解质电离平衡常数分析一水合氨的电离平衡常数。
(1)氯化铝溶液和碳酸钠溶液混合,发生盐的双水解反应,产生白色氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;
(2)据图分析,加水稀释的过程中,HX的pH变化比较小,说明HX的酸性比醋酸弱,酸性越弱,在相同外界条件下,酸的电离平衡常数越小,所以HX的电离平衡常数小于醋酸的电离平衡常数;
根据电荷守恒,c(CH3COO-)+c(OH-)=c(Na+)+c(H+),c(X-)+c(OH-)=c(Na+)+c(H+),即离子总数是c(Na+)+c(H+)的2倍,而NaX的水解程度大,即NaX溶液中的c(OH-)大,则其溶液中c(H+)小,而c(Na+)相同,所以乙酸钠中离子总浓度大些;
(3)①25 ℃时,HCN的电离平衡常数Ka=4.9×10-10,而NaCN的水解平衡常数Kh=![]() =2.0×10-5> Ka=4.9×10-10,水解程度大于其电离程度,所以溶液显碱性;CN-水解产生HCN,所以微粒浓度c(HCN)>c(CN-);
=2.0×10-5> Ka=4.9×10-10,水解程度大于其电离程度,所以溶液显碱性;CN-水解产生HCN,所以微粒浓度c(HCN)>c(CN-);
②25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中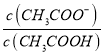 =
=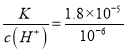 =18;
=18;
(4)在25°C下,将x mol·L-1的氨水与y mol·L-1的盐酸等体积混合,反应后溶液中显中性,在该溶液中存在电荷守恒,c(H+)+c(NH4+)=c(Cl-)+c(OH-),由于溶液显中性,所以c(H+)=c(OH-),则c(NH4+)=c(Cl-);NH3·H2O在溶液中存在电离平衡:NH3·H2O![]() NH4++OH-,NH3·H2O的电离平衡常数K=
NH4++OH-,NH3·H2O的电离平衡常数K=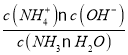 =
=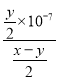 =
=![]() 。
。

【题目】乙烯是一种重要的基本化工原料,实验小组同学欲制备乙烯并验证其与溴单质的反应类型为加成反应。
I.乙烯的制备
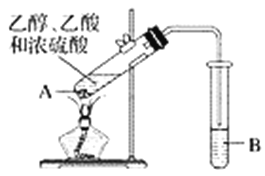
欲利用下图所给装置制备乙烯。反应原理为:CH3CH2OH ![]() CH2=CH2↑+H2O,反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
CH2=CH2↑+H2O,反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
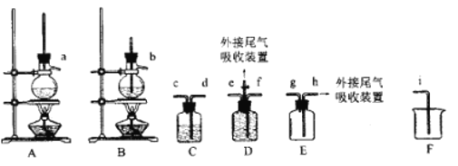
(1)欲收集一瓶乙烯,选择上图中的装置,其连接顺序为_____(按气流方向,用小写字母表示)。
(2)C中盛放的试剂为______,其作用为_____。
(3)在烧杯中混合浓硫酸和乙醇时,应先添加___;实验开始一段时间后发现忘记加碎瓷片,此时应该进行的操作为____。
(4)尾气吸收可采用________(填选项字母)。
A.KMnO4酸性溶液 B.浓硫酸 C.饱和Na2CO3溶液 D.NaOH溶液
II.验证乙烯与溴单质的反应类型为加成反应。
实验小组同学将I中制得的乙烯干燥后,按下列两种方案进行实验。
方案 | 操作 | 现象 |
一 | 将纯净的乙烯通入溴水中 | 溴水褪色 |
二 | 向充满纯净乙烯的塑料瓶中注入适量溴的CC14溶液,振荡 | ①溴的CCl4溶液褪色 ② |
(5)乙烯与溴单质发生加成反应的化学方程式为_________。
(6)方案一不能证明乙烯与溴单质发生了加成反应,原因为_________。
(7)方案二中现象②应为______,要想用此方案证明乙烯与溴单质发生的反应是加成反应,还需补充的实验为:继续向方案二塑料瓶中加入少量______,振荡后,若_____,证明发生了加成反应。