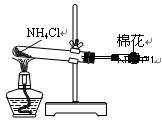
题目内容
下列实验不能达到预期目的的是 ( )
| 序号 | 实验操作 | 实验目的 |
| A | 浓、稀HNO3分别与Cu反应 | 比较浓、稀HNO3的氧化性强弱 |
| B | MgCl2、AlCl3浓液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | 测定等浓度的Na3PO4、Na2SO4两溶液的PH | 比较磷、硫的非金属性强弱 |
| D | 用等浓度的盐酸、碳酸氢钠两溶液混合反应 | 比较盐酸、碳酸的酸性强弱 |
B
本题考查实验分析能力;HNO3浓度不同,与铜反应的速率不同,产物不同,浓硝酸的氧化性大于稀硝酸,A可达到实验目的;MgCl2、AlCl3浓液中分别通入NH3,都会产生白色沉淀,氢氧化铝不溶于弱碱,不能比较其金属性强弱;B不能达到实验目的;Na3PO4是强碱弱酸盐,Na2SO4是强酸强碱盐,等浓度的两溶液,Na3PO4的pH大于Na2SO4的pH,可知P的非金属性<S,C可达到实验目的;用等浓度的盐酸、碳酸氢钠两溶液混合,可生成无色气体CO2,说明了强酸HCl制弱酸H2CO3,D可达到实验目的。

练习册系列答案
相关题目
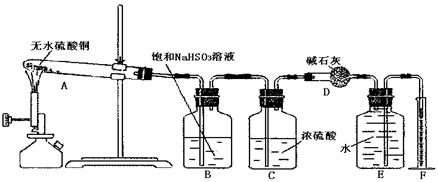
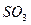 被
被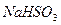 溶液吸收时产生了
溶液吸收时产生了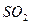 气体
气体 出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。
出氧气的体积为224mL(标准状况)。据此可计算出二氧化硫为 mol,三氧化硫为 mol。 溶度积/25℃
溶度积/25℃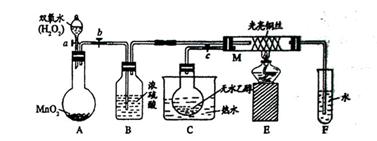
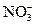 、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是