题目内容
有A、B、C、D四种短周期的非金属元素(其单质也分别用A、B、C、D表示),原子序数按A、B、C、D顺序依次增大,A原子核外只有一种运动状态的电子,B原子核外有3个未成对电子,B、C元素在周期表中是同周期的相邻元素,D与B、C处于不同周期.
甲、乙、丙、丁、戊是以上四种元素组成的化合物,其中甲由A、C组成,乙由A、D组成,丁由A、B组成,乙的浓溶液与一种黑色粉末共热可得单质D.它们有如下的变化关系: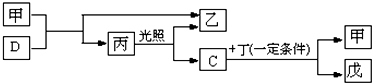
回答下列问题:
(1)元素D在周期表的位置是 ,它的原子核外共有 种不同能量的电子;
(2)上述化合物中,10电子的分子有 (写化学式);
(3)乙和丁反应后生成的物质中存在的化学键有 ;
(4)单质C与甲、戊反应总化学方程式: .
甲、乙、丙、丁、戊是以上四种元素组成的化合物,其中甲由A、C组成,乙由A、D组成,丁由A、B组成,乙的浓溶液与一种黑色粉末共热可得单质D.它们有如下的变化关系:

回答下列问题:
(1)元素D在周期表的位置是
(2)上述化合物中,10电子的分子有
(3)乙和丁反应后生成的物质中存在的化学键有
(4)单质C与甲、戊反应总化学方程式:
考点:无机物的推断,位置结构性质的相互关系应用
专题:推断题,元素周期律与元素周期表专题
分析:A原子核外只有一种运动状态的电子,则A为H元素,B原子核外有3个未成对电子,则最外层电子应有5个,为ns2np3排布,为ⅤA族元素,B、C元素在周期表中是同周期的相邻元素,C为ⅥA族元素,D与B、C处于不同周期,则说明B、C为第二周期,B为N元素,C为O元素,乙的浓溶液与一种黑色粉末共热可得单质D,通常为浓盐酸与二氧化锰的反应,D为Cl元素,单质D为氯气,甲由A、C组成,应为H2O.乙为HCl,则丙为HClO,丁由A、B组成,应为NH3,则戊为NO,以此解答该题.
解答:
解:A原子核外只有一种运动状态的电子,则A为H元素,B原子核外有3个未成对电子,则最外层电子应有5个,为ns2np3排布,为ⅤA族元素,B、C元素在周期表中是同周期的相邻元素,C为ⅥA族元素,D与B、C处于不同周期,则说明B、C为第二周期,B为N元素,C为O元素,乙的浓溶液与一种黑色粉末共热可得单质D,通常为浓盐酸与二氧化锰的反应,D为Cl元素,单质D为氯气,甲由A、C组成,应为H2O.乙为HCl,则丙为HClO,丁由A、B组成,应为NH3,则戊为NO,
(1)由以上分析可知D为Cl元素,位于周期表第三周期第ⅧA族,原子核外有1s、2s、2p、3s、3p等5种能量不同的电子,
故答案为:第三周期第ⅧA族;5;
(2)上述化合物中,10电子的分子有H2O、NH3,故答案为:H2O、NH3;
(3)乙和丁反应后生成的物质氯化铵,含有离子键和共价键,故答案为:离子键、共价键;
(4)单质C与甲、戊反应总化学方程式4NO+3O2+2H2O=4HNO3,故答案为:4NO+3O2+2H2O=4HNO3.
(1)由以上分析可知D为Cl元素,位于周期表第三周期第ⅧA族,原子核外有1s、2s、2p、3s、3p等5种能量不同的电子,
故答案为:第三周期第ⅧA族;5;
(2)上述化合物中,10电子的分子有H2O、NH3,故答案为:H2O、NH3;
(3)乙和丁反应后生成的物质氯化铵,含有离子键和共价键,故答案为:离子键、共价键;
(4)单质C与甲、戊反应总化学方程式4NO+3O2+2H2O=4HNO3,故答案为:4NO+3O2+2H2O=4HNO3.
点评:本题综合考查元素元素周期比与元素化合物推断,难度较大,推断元素是关键,是对所学知识的综合运用与学生能力考查,注意基础知识的掌握.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式的是( )
| A、氧化亚铁与稀硝酸反应:FeO+2H+═Fe2++H2O |
| B、氢氧化钡与稀硫酸反应:Ba2++SO42-﹦BaSO4↓ |
| C、铜与浓硝酸反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D、氯化铵溶液加入氢氧化钠溶液:NH4++OH-=NH3↑+H2O |
下列元素中,金属性最强的是( )
| A、K | B、Al | C、He | D、S |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,0.56L丙烷中含有共价键的数目为0.2NA |
| B、0.1mol H2O和D2O组成的混合物中含有的中子数是NA |
| C、标准状况下,2.24L Cl2溶于水,转移的电子数目为0.1NA |
| D、常温下,20L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.