题目内容
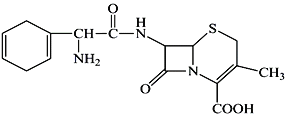
【题目】某高分子化合物R的结构简式如下,下列有关R的说法正确的是( )
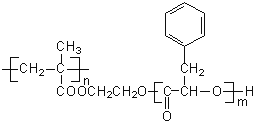
A. R的单体之一的分子式为C9H10O2
B. R完全水解后生成物均为小分子有机物
C. 通过加聚反应和缩聚反应可以生成R
D. 碱性条件下,1molR完全水解消耗NaOH的物质的量为2nmol
【答案】C
【解析】
A. 由R的结构简式可知,合成R的分子分别是2-甲基丙烯酸、乙二醇和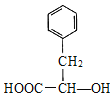 ,分子式为C4H6O2、C2H6O2、C9H10O3,故A项错误;
,分子式为C4H6O2、C2H6O2、C9H10O3,故A项错误;
B.R完全水解,除了小分子有机物外还有高分子化合物 生成,故B项错误;
生成,故B项错误;
C. R前面的链节是通过碳碳双键发生加聚反应制得,后面的链节则是羧基跟羟基通过缩聚反应制得的,故C项正确;
D. 1molR中含n(1+m)mol酯基,1molR完全水解消耗NaOH的物质的量为n(1+m)mol,故D项错误;
故选C。

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
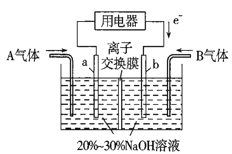
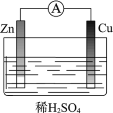
【题目】某原电池装置如图所示。其中,Zn电极为原电池的______极(填“正”或“负”),电极反应式是______________。Cu电极上发生的反应属于______(填“氧化”或“还原”) 反应。
【题目】下列实验操作、现象及结论均正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 黄色溶液中只含Br2 |
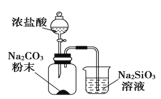
B | 烧杯中看见白色沉淀 | 证明酸性强弱:H2CO3>H2SiO3 |
C | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液;未出现银镜 | 蔗糖未水解 |
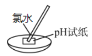
D | pH试纸先变红后褪色 | 氯水既有酸性,又有漂白性 |
A.AB.BC.CD.D