题目内容
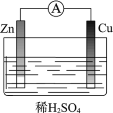
【题目】(1)在第三周期元素及其单质和化合物中,原子半径最小的元素是________(用元素符号或化学式表示,下同);氧化性最强的单质是________;还原性最强的单质是________;最高价氧化物对应的水化物中酸性最强的是________;碱性最强的是________;形成的两性氢氧化物是________。
(2)在某温度下,于密闭容器中进行下列反应:2SO2(气)+O2(气)![]() 2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,这时c(SO2)=________mol/L,c(O2)=________mol/L,c(SO3)=________mol/L
2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,这时c(SO2)=________mol/L,c(O2)=________mol/L,c(SO3)=________mol/L
(3)燃烧11.2L(标准状况)甲烷,生成二氧化碳的物质的量为________,生成水的质量为________。
【答案】Cl Cl2 Na HClO4 NaOH Al(OH)3 0.6 0.8 2.4 0.5mol 18g
【解析】
同周期除0族元素外,从左到右,原子半径逐渐减小,单质氧化性逐渐增强、还原性逐渐减弱,最高价氧化物对应水合物酸性逐渐增强、碱性逐渐减弱。
(1)综上分析,在第三周期元素及其单质和化合物中,原子半径最小的元素是Cl;氧化性最强的单质是Cl2;还原性最强的单质是Na;Cl元素的最高价氧化物对应的水化物酸性最强,化学式为HClO4;Na元素的最高价氧化物对应的水化物碱性最强,化学式为NaOH;第三周期中Al(OH)3为两性氢氧化物。
(2) 在某温度下,于密闭容器中进行下列反应:2SO2(气)+O2(气)![]() 2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,则SO2反应了的浓度为80%
2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,则SO2反应了的浓度为80%![]() 3mol/L=2.4 mol/L,氧气反应的浓度为1.2 mol/L,生成的三氧化硫的浓度为2.4 mol/L,故此时c(SO2)=(3-2.4)mol/L =0.6mol/L,c(O2)=(2-1.2) mol/L=0.8mol/L,c(SO3)=2.4mol/L。
3mol/L=2.4 mol/L,氧气反应的浓度为1.2 mol/L,生成的三氧化硫的浓度为2.4 mol/L,故此时c(SO2)=(3-2.4)mol/L =0.6mol/L,c(O2)=(2-1.2) mol/L=0.8mol/L,c(SO3)=2.4mol/L。
(3) 11.2L(标准状况)甲烷的物质的量为![]() ,根据甲烷的分子式CH4可知,生成二氧化碳的物质的量为0.5mol,生成水的质量为
,根据甲烷的分子式CH4可知,生成二氧化碳的物质的量为0.5mol,生成水的质量为![]() 。
。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案