题目内容
对体积不变的气体反应,升高温度时,化学反应速率加快,主要原因是( )
| A、分子运动速率加快,使反应物分子间的碰撞机会增多 |
| B、反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C、该反应的过程是吸热的 |
| D、该反应的过程是放热的 |
考点:浓度、温度、催化剂对化学反应速率的影响
专题:
分析:对体积不变的气体反应,根据升高温度,活化分子百分数的增多,从而使有效碰撞次数增多来分析.
解答:
解:对体积不变的气体反应,升高温度时,化学反应速率加快,是因升高温度,反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多,化学反应速率加快,而与该反应为吸热反应或放热反应无关,
故选B.
故选B.
点评:本题考查化学反应速率的影响,为高考高频考点,侧重于学生的基础知识的考查,有利于夯实双基,培养学生的学习积极性,难度不大.注意升高温度,反应物中活化分子的百分数增大,化学反应速率增大.

练习册系列答案
相关题目
下列各组离子,在指定环境中能大量共存的是( )
| A、常温下,在PH>7的溶液中,Na+、S2-、K+、AlO2- |
| B、常温下,在PH>1的溶液中,SO32-、S2-、K+、NH4+ |
| C、常温下,在PH=1的溶液中,Fe2+、HCO3-、Na+、SO42- |
| D、常温下,在PH<7的溶液中,Fe3+、Cu2+、Cl-、NO3- |
下列各项表达式正确的是( )
A、S原子的结构示意图: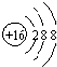 |
| B、过氧化钠的结构式:Na-O-O-Na |
| C、K+离子的核外电子排布式:1s22s22p63s23p6 |
| D、丙烯酸(CH2=CHCOOH)分子中含9个σ键,1个π键 |
已知有如下反应,对下列氧化性和还原性的强弱判断正确的是( )
①2Fe3++2I-═2Fe2++I2
②2Fe2++Br2═2Fe3++2Br-
③2Fe(CN)64-+I2═2Fe(CN)63-+2I-.
①2Fe3++2I-═2Fe2++I2
②2Fe2++Br2═2Fe3++2Br-
③2Fe(CN)64-+I2═2Fe(CN)63-+2I-.
| A、氧化性:Fe3+>Br2>I2>Fe(CN)63- |
| B、还原性:Fe(CN)64->I->Fe2+>Br- |
| C、氧化性:Br2>Fe3+>I2>Fe(CN)63- |
| D、还原性:Fe(CN)64->Fe2+>I->Br- |
下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150mL 2mol/L KCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、75mL 1mol/L AlCl3溶液 |
一定条件下,通过下列反应可实现燃煤烟气中的硫的回收:SO2(g)+2CO(g)?2CO2(g)+S(l)△H<0
一定温度下,在容积为2L的恒容密闭容器中充入1mol SO2和n mol CO发生反应,5min后达到平衡,生成2a mol CO2.下列说法正确的是( )
一定温度下,在容积为2L的恒容密闭容器中充入1mol SO2和n mol CO发生反应,5min后达到平衡,生成2a mol CO2.下列说法正确的是( )
| A、平衡后保持其它条件不变,从容器中分离出部分硫,平衡向正反应方向移动 |
| B、当混合气体的物质的量不再改变时,反应达到平衡状态 |
| C、平衡后保持其它条件不变,升高温度和加入催化剂,SO2的转化率均增大 |
| D、反应前2min的平均速率v(SO2)=0.1a mol/(L?min) |
能正确表示下列化学反应的离子方程式的是( )
| A、碳酸钙溶于稀盐酸中:CO32-+2H+=H2O+CO2↑ |
| B、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、氢氧化钡溶液与盐酸的反应:OH-+H+=H2O |
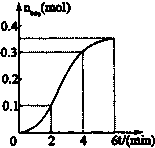 已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A、反应开始后2~4分钟内平均反应速率最大 |
| B、反应刚开始时反应速率较小,然后逐渐增大 |
| C、反应前阶段速率逐渐增大,是因为反应放热,使反应速率加快 |
| D、生成物CaCl2、CO2和H2O的总能量比反应物CaCO3和盐酸的总能量高 |