��Ŀ����
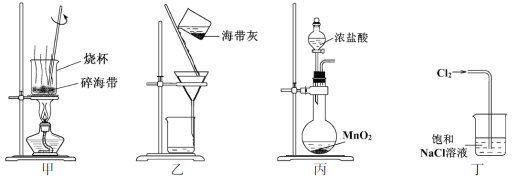
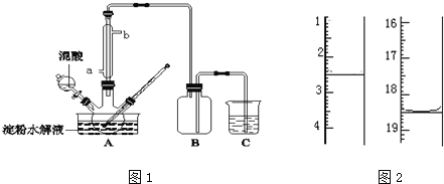
����Ŀ������ͼ�ڳİ�ֽ�IJ���Ƭ�������������KMnO4����������Χ�ֱ�μ�һ�κ��з�̪�ij���ʯ��ˮ��FeCl2��Һ��Ȼ����KMnO4�����ϵμ�������Ũ���ᣬѸ�ٸǺñ�����
��ʾ��ʵ���������õ�������������������ԭ����ȡ��

2KMnO4��16HCl��Ũ��=2KCl��2MnCl2��5Cl2����8H2O���˷�Ӧ�ڳ����¼��ܽ��С�
(1)�������뻹ԭ�����ʵ���֮��Ϊ____________ ����������Ϊ____________��
(2)����0��1 mol Cl2����ת�Ƶ��ӵ����ʵ���Ϊ ______ mol��
(3)a����Ӧ�Ļ�ѧ����ʽ�ǣ���ҵ���ô�ԭ����ȡƯ�ۡ���______________________��
(4)b�����ӷ���ʽ��_______________________________________________��
(5)������ر���Һ���������ζ��������ʵĺ������ø�����ط���Ӳⶨʯ��ʯ��CaCO3�ĺ����ķ���Ϊ: ��ȡ����0��1250g����ϡ�����ܽ�����(NH4)2C2O4��CaC2O4����������������ϴ�Ӻ�����ϡ�����С��ζ����ɵ�H2C2O4 ��ȥŨ��Ϊ0��016mo/LKMnO4��Һ25��00mL��
��д��CaC2O4�����ܽ�����ӷ���ʽ:__________________________
����ƽ��������и�����صζ����ᷴӦ�����ӷ���ʽ:
_____MnO4-+______H2C2O4+______ H+=____Mn2++_____CO2��+_____ ________
���𰸡�1:5 Cl2 0.2 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O 2Fe2+��Cl2=2Fe3����2Cl���� CaC2O4(s) + 2H+(aq) + SO42(aq) ![]() CaSO4(s) + H2C2O4(aq) 2 5 6 2 10 8 H2O
CaSO4(s) + H2C2O4(aq) 2 5 6 2 10 8 H2O
��������
(1)����������ԭ��Ӧ�л��ϼ۱仯���ҳ�����������ԭ�������ǵ����ʵ�����
(2)���ݷ���ʽ����ת�Ƶ�����Ŀ��
(3)a����Ӧ���������������Ʒ�Ӧ�����Ȼ��ơ�������ƺ�ˮ��
(4)b�����������Ȼ�������Ӧ�����Ȼ�����
(5)��CaC2O4�����ܽ���һ�������ܽ�ƽ��ת����CaC2O4(s)��H2SO4(aq)��Ӧ����CaSO4(s)��H2C2O4(aq)���ڸ����������5����̬��������ÿ��̼����1����̬��������2����̬�����ݵ�ʧ�����غ���ƽ��
(1) KMnO4��Mn���ϼ۽��ͣ�Ϊ����������2mol��������HCl��Cl���ϼ����ߣ�Ϊ��ԭ����16mol HCl���뷴Ӧ����ֻ��10molHCl���ߣ���ԭ��Ϊ10mol������������뻹ԭ�����ʵ���֮��Ϊ2:10 =1:5�����ϼ����ߵõ��IJ���Ϊ������������������ΪCl2���ʴ�Ϊ��1:5��Cl2��
(2)���ݷ���ʽ֪ת��10mol��������5mol Cl2����˲���0.1 mol Cl2��ת�Ƶ��ӵ����ʵ���Ϊ0.2 mol���ʴ�Ϊ:0.2��
(3)a����Ӧ���������������Ʒ�Ӧ�����Ȼ��ơ�������ƺ�ˮ���仯ѧ����ʽ��2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O���ʴ�Ϊ��2Cl2+2Ca(OH)2 = CaCl2+ Ca(ClO)2 + 2H2O��
(4)b�����������Ȼ�������Ӧ�����Ȼ����������ӷ���ʽ��2Fe2+��Cl2 = 2Fe3����2Cl�����ʴ�Ϊ��2Fe2+��Cl2 = 2Fe3����2Cl����
(5)��CaC2O4�����ܽ���һ�������ܽ�ƽ��ת����CaC2O4(s)��H2SO4(aq)��Ӧ����CaSO4(s)��H2C2O4(aq)�������ӷ���ʽ��CaC2O4(s) + 2H+(aq) + SO42(aq) ![]() CaSO4(s) + H2C2O4(aq)���ʴ�Ϊ��CaC2O4(s) + 2H+(aq) + SO42(aq)
CaSO4(s) + H2C2O4(aq)���ʴ�Ϊ��CaC2O4(s) + 2H+(aq) + SO42(aq) ![]() CaSO4(s) + H2C2O4(aq)��
CaSO4(s) + H2C2O4(aq)��
�ڸ����������5����̬��������ÿ��̼����1����̬��������2����̬�����ݵ�ʧ�����غ���ƽ�õ�������صζ����ᷴӦ�����ӷ���ʽ��2MnO4�� + 5 H2C2O4 + 6 H+ = 2 Mn2++ 10 CO2��+ 8 H2O���ʴ�Ϊ��2��5��6��2��10��8��H2O��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���ߴ���������Ϊ�ϳ���������Ԫ�������ϵ�ԭ�ϣ���ҵ�Ͽ�����Ȼ�������̷������̿���Fe��Al��Mg��Zn��Ni��Si��Ԫ��������Ʊ�����������ͼ��ʾ���ش��������⣺
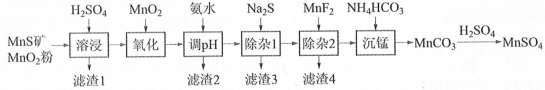
��ؽ�������[c0(Mn+)=0.1 molL1]�γ��������������pH��Χ���£�
�������� | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
��ʼ������pH | 8��1 | 6��3 | 1��5 | 3��4 | 8��9 | 6��2 | 6��9 |
������ȫ��pH | 10��1 | 8��3 | 2��8 | 4��7 | 10��9 | 8��2 | 8��9 |
(1)������1������S��__________________________��д�����ܽ����ж������������̷�Ӧ�Ļ�ѧ����ʽ____________________________________________________��
(2)��������������������MnO2�������ǽ�________________________��
(3)����pH��������������Һ��pH��ΧӦ����Ϊ_______~6֮�䡣
(4)д�������̡������ӷ���ʽ_____________��
(5)��״��������Ԫ���Ͽ���Ϊ����ӵ���������ϣ��仯ѧʽΪLiNixCoyMnzO2������Ni��Co��Mn�Ļ��ϼ۷ֱ�Ϊ+2��+3��+4����x=y=![]() ʱ��z=__________��
ʱ��z=__________��