题目内容
2.下列推断正确的是( )| A. | 硅是地壳中含量位居第二的元素,玛瑙、光导纤维的主要成分为SiO2 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 加碘食盐中加入的是碘单质,可防止甲状腺肿大疾病 | |
| D. | 要除去衣服上的顽固污渍,均可将衣服泡在漂白液中 |
分析 A.地壳元素含量前四位为:O、si、Al、Fe,中含量位居第二的元素是硅,玛瑙、光导纤维的主要成分为SiO2;
B.绿色化学的核心是要利用化学原理从源头消除污染,实现零排放;
C.加碘食盐中加入的是碘酸钾;
D.漂白液能把衣服全部漂白.
解答 解:A.地壳中含量位居第二的元素是硅,玛瑙、光导纤维的主要成分为SiO2,故A正确;
B.绿色化学的核心是要利用化学原理从源头消除污染,实现零排放,而不是对环境污染进行治理,故B错误;
C.加碘食盐中加入的是碘酸钾,不是碘单质,故C错误;
D.将衣服泡在漂白液不但能除去衣服上的顽固污渍,而且能把衣服全部漂白,故D错误;
故选:A.
点评 本题考查了硅的含量及其化合物、绿色化学的概念、次氯酸的漂白性,熟悉物质性质是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.一般情况下,前者无法决定后者的是( )
| A. | 原子核外电子排布--元素在周期表中的位置 | |
| B. | 弱电解质的相对强弱--电离常数的大小 | |
| C. | 分子间作用力的大小--分子稳定性的高低 | |
| D. | 物质内部储存的能量--化学反应的热效应 |
15.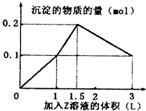 某混合溶液中,含溶质X、Y各0.1mol,向其中滴加0.1mol/L的Z溶液,所得沉淀的物质的量如图,则符合条件的X、Y、Z分别是( )
某混合溶液中,含溶质X、Y各0.1mol,向其中滴加0.1mol/L的Z溶液,所得沉淀的物质的量如图,则符合条件的X、Y、Z分别是( )
 某混合溶液中,含溶质X、Y各0.1mol,向其中滴加0.1mol/L的Z溶液,所得沉淀的物质的量如图,则符合条件的X、Y、Z分别是( )
某混合溶液中,含溶质X、Y各0.1mol,向其中滴加0.1mol/L的Z溶液,所得沉淀的物质的量如图,则符合条件的X、Y、Z分别是( )| A. | 偏铝酸钠、氢氧化钡、硫酸 | B. | 偏铝酸钠、氯化钡、硫酸 | ||
| C. | 氯化铝、氯化镁、氢氧化钠 | D. | 氯化铝、氯化铁、氢氧化钠 |
12.分子式为C6H14O的醇有多种结构,其中能经过两步氧化生成羧酸的结构有(不考虑立体异构)( )
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
14.下列说法正确的是( )
| A. | 结构片段为 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 | |
| B. | 等质量的乙烯、乙醇、丙烯酸(CH2=CH-COOH)完全燃烧消耗氧气的量相等 | |
| C. | 由甘氨酸、丙氨酸形成的二肽有三种 | |
| D. | 石油的裂化、煤的汽化与液化都属于化学变化,而石油的分馏与煤的干馏都属于物理变化 |
 铜及其化台物在工业、农业、科技和日常生活中有广泛应用.
铜及其化台物在工业、农业、科技和日常生活中有广泛应用.