题目内容
【题目】把400mLNH4HCO3和Na2CO3的混合溶液分成两等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
A. (b/10-a/20)mol/L B. (2b-a)mol/L C. (5b-5a/2)mol/L D. (10b-5a)mol/L
【答案】C
【解析】
NH4HCO3和Na2CO3的混合溶液加入NaOH,反应为NH4HCO3+2NaOH=NH3H2O+Na2CO3+H2O,加入HCl的盐酸反应为NH4HCO3+HCl=NH4Cl+CO2↑+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑,根据方程式计算。
把400mLNH4HCO3和Na2CO3的混合溶液分成两等份,每一份溶液的体积为200mL。设在200ml溶液中含有NH4HCO3xmol,Na2CO3ymol,NH4HCO3和Na2CO3的混合溶液加入amolNaOH,反应为NH4HCO3+2NaOH=NH3H2O+Na2CO3+H2O,n(NH4HCO3)=n(NaOH)=0.5amol,另一等份溶液中加入含bmolHCl的盐酸的反应为NH4HCO3+HCl=NH4Cl+CO2↑+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑,根据第一个方程式中物质间的关系可知n(HCl)= n(NaOH)=0.5amol,则与Na2CO3发生反应消耗HCl的物质的量为(b-0.5a)mol,根据二者反应时的物质的量关系可知:n(Na2CO3)的物质的量为n(Na2CO3)=![]() ,则该份溶液中含有的钠离子物质的量n(Na+)=2n(Na2CO3)=(b-0.5a)mol,由于溶液的体积为200mL,故c(Na+)=
,则该份溶液中含有的钠离子物质的量n(Na+)=2n(Na2CO3)=(b-0.5a)mol,由于溶液的体积为200mL,故c(Na+)=![]() mol/L,选项C符合题意。
mol/L,选项C符合题意。

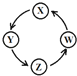
【题目】下列各组物质中,满足表中图示物质在一定条件下能一步转化的组合有
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Al | AlCl3 | Al(OH)3 | Al2O3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ②③ B. ①③④ C. ①④ D. ①②③
【题目】下表是元素周期表的一部分,请回答有关问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 ________ ;
(2)表中能形成两性氢氧化物的元素是 ________ (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式:_________;
(3)③⑦⑩三种元素的阴离子还原性顺序为: ___________________;⑦的水溶液呈__________色 ;
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 _______(填化学式) ;
(5)③元素与⑩元素两者核电荷数之差是 ____________ ;
(6)设计实验方案:比较⑦与⑥单质氧化性的强弱,请将方案填入下表。
实验步骤 | 实验现象与结论 |
____________________ | ____________________ |