��Ŀ����
10�������ơ���һ���ڻ�ѧѧϰ�г��õķ������������ƽ�������ȷ���ǣ�������| A�� | ��A��Ԫ���⻯���۵�˳��GeH4��SiH4��CH4�����A��Ԫ���⻯���۵�˳��ҲӦΪ��H2Se��H2S��H2O | |
| B�� | ��2����Ԫ���⻯����ȶ���˳����HF��H2O��NH3�����3����Ԫ���⻯����ȶ���˳��Ҳ��HCl��H2S��PH3 | |
| C�� | ��Ϊ����ɫ��֪�������������ɫ | |
| D�� | BaCl2��Һ��ͨ��SO2������������Ba��NO3��2��Һ��ͨ��SO2Ҳ�������� |
���� A��H2O���Ӽ����������۵�ϸߣ�
B���ǽ�����Խǿ���⻯��Խ�ȶ���
C��Cs����ɫ���Խ�ɫ��
D�����������£�����������ܰѶ�����������Ϊ�������
��� �⣺A����A��Ԫ���⻯���۵�˳��GeH4��SiH4��CH4��H2O���Ӽ����������۵�ϸߣ����A��Ԫ���⻯���۵�˳��Ϊ��H2O��H2Se��H2S����A����
B���ǽ�����Խǿ���⻯��Խ�ȶ����ǽ�����F��O��N��Cl��S��P�����⻯����ȶ��ԣ�HF��H2O��NH3��HCl��H2S��PH3����B��ȷ��
C��NaΪ��ɫ������Cs����ɫ���Խ�ɫ��������ɫ��ͬ����C����
D��BaCl2��Һ��ͨ��SO2�������������������£�����������ܰѶ�����������Ϊ�����������Ba��NO3��2��Һ��ͨ��SO2���������ᱵ��������D����
��ѡB��
���� ���⿼����Ԫ�������ɡ��������������������ʡ�����ȣ���Ŀ�漰��֪ʶ��϶࣬�����ڻ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ���

��ϰ��ϵ�д�
 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
�����Ŀ
20�����ʵ���Ũ����ͬʱ�����м��ܸ�NaOH��Һ��Ӧ�����ܸ�������Һ��Ӧ����Һ�У�pH�����ǣ�������
| A�� | Na2CO3��Һ | B�� | Na[Al��OH��4]��Һ | C�� | NaHCO3��Һ | D�� | NaHSO3��Һ |
1���ݱ�����п��ؿ���ȡ��Ŀǰ�㷺ʹ�õ�Ǧ���أ���Ϊп�����������û��Ǧ��Ⱦ�����ط�ӦΪ2Zn+O2�T2ZnO��ԭ��Ϊп�������Һ�Ϳ�����������������ȷ���ǣ�������
| A�� | пΪ�������������븺����Ӧ | B�� | ������ӦΪZn-2e-�TZn2+ | ||
| C�� | �����Ϸ���������Ӧ | D�� | ���Һ������������Һ |
18�� ������о���Ա������һ�ִ�����Ũ����ȩ��ˮ���·���-��Ĥ��ⷨ����ȩ�ֱ�����������������Ӧ��ת��Ϊ�Ҵ������ᣮʵ������һ��Ũ�ȵ���ȩ-Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ������˵����ȷ���ǣ�������
������о���Ա������һ�ִ�����Ũ����ȩ��ˮ���·���-��Ĥ��ⷨ����ȩ�ֱ�����������������Ӧ��ת��Ϊ�Ҵ������ᣮʵ������һ��Ũ�ȵ���ȩ-Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ������˵����ȷ���ǣ�������
 ������о���Ա������һ�ִ�����Ũ����ȩ��ˮ���·���-��Ĥ��ⷨ����ȩ�ֱ�����������������Ӧ��ת��Ϊ�Ҵ������ᣮʵ������һ��Ũ�ȵ���ȩ-Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ������˵����ȷ���ǣ�������
������о���Ա������һ�ִ�����Ũ����ȩ��ˮ���·���-��Ĥ��ⷨ����ȩ�ֱ�����������������Ӧ��ת��Ϊ�Ҵ������ᣮʵ������һ��Ũ�ȵ���ȩ-Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ����CH4-����ȼ�ϵ��Ϊֱ����Դ��ȼ�ϵ�ص�b��Ӧͨ����� | |
| B�� | �������У�����0.1 mol�����ͬʱ����0.2 mol���Ҵ����� | |
| C�� | ������ӦCH3CHO-2e-+OH-�TCH3COOH+H+ | |
| D�� | ���������������ֱ�����������Ҵ��⣬����������ɫ���壬��������������O2 |
5�����и����У�ÿ�ֵ������Һ���ʱ���ˮ���͵��ǣ�������
| A�� | HCl��CuCl2��Ba��OH��2 | B�� | NaOH��CuSO4��H2SO4 | ||
| C�� | NaOH��H2SO4��Ba��OH��2 | D�� | NaBr��H2SO4��Ba��OH��2 |
2���ҹ�������������Ӧ��ʪ��ұ����ұ���Ľ����ǣ�������
| A�� | Fe | B�� | Cu | C�� | Ag | D�� | Hg |
20��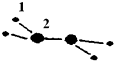 ��1��M�����ֶ�����Ԫ����ɣ�ÿ��M���Ӻ���18�����ӣ���������ģ����ͼ��ʾ�����M��Ħ������Ϊ32g/mol���������Ϊ2��ԭ�ӽṹʾ��ͼ��
��1��M�����ֶ�����Ԫ����ɣ�ÿ��M���Ӻ���18�����ӣ���������ģ����ͼ��ʾ�����M��Ħ������Ϊ32g/mol���������Ϊ2��ԭ�ӽṹʾ��ͼ��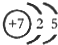 ��
��
��2����֪1.0mol•L-1NaHSO3��Һ��pHΪ3.5��������ˮ������ҺpHѸ�ٽ��ͣ���ҺpH���͵�ԭ����HSO3-+Cl2+H2O=3H++SO42-+2Cl-�������ӷ���ʽ��ʾ����
��3���ڳ��³�ѹ���������£�N2�ڴ�����TiO2��������H2O��Ӧ������1molNH3��O2ʱ�������仯ֵΪ382.5kJ���ﵽƽ���˷�ӦNH3���������¶ȵ�ʵ���������±�����÷�Ӧ���Ȼ�ѧ����ʽΪ$\frac{1}{2}$N2��g��+$\frac{3}{2}$H2O��l��?NH3��g��+$\frac{3}{4}$O2��g����H=+382.5kJ/mol����2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol����
��4������Һ�У�һ��Ũ�ȵ�NH4+���ܽⲿ��Mg��OH��2���壬��Ӧ���£�
2NH4+��aq��+Mg��OH��2��s��?Mg2+��aq��+2NH3•H2O��aq��
д��������Ӧ��ƽ�ⳣ������ʽK=$\frac{c��M{g}^{2+}��•{c}^{2}��N{H}_{3}•{H}_{2}O��}{{c}^{2}��N{{H}_{4}}^{+}��}$
ij�о���ѧϰС��Ϊ̽��Mg2+��NH3•H2O��Ӧ�γɳ���������������������ʵ��
�����ʵ��١��ڲ�����ͬ�����ԭ��ƽ�����ʽ���Կ�������c��NH3•H2O����c��Mg2+���ı���ͬ�ij̶ȣ�c2��NH3•H2O���Գ������ɵ�Ӱ�����[�����c��Mg2+��•c2��OH-����Ksp[Mg��OH��2]��������c��Mg2+��•c2��OH-����Ksp[Mg��OH��2]��
��5���������£���ѧ��ӦI-��aq��+ClO-��aq��=IO-��aq��+Cl-��aq���ķ�Ӧ���ʼŨ�ȡ���Һ�е����������ӳ�ʼŨ�ȼ���ʼ���ʼ�Ĺ�ϵ���±���ʾ��
��֪���г�ʼ��Ӧ�������й�����Ũ�ȹ�ϵ���Ա�ʾΪv=k[I-]1[ClO-]b[OH-]c���¶�һ��ʱ��kΪ��������
�����ʵ��2��ʵ��4��Ŀ����̽��ClO-�Է�Ӧ���ʵ�Ӱ�죻
����ʵ����4������Ũ�Ȳ��䣬������Һ�����ֵ���ΪpH=13����Ӧ�ij�ʼ����v=7.2��10-4��
 ��1��M�����ֶ�����Ԫ����ɣ�ÿ��M���Ӻ���18�����ӣ���������ģ����ͼ��ʾ�����M��Ħ������Ϊ32g/mol���������Ϊ2��ԭ�ӽṹʾ��ͼ��
��1��M�����ֶ�����Ԫ����ɣ�ÿ��M���Ӻ���18�����ӣ���������ģ����ͼ��ʾ�����M��Ħ������Ϊ32g/mol���������Ϊ2��ԭ�ӽṹʾ��ͼ�� ��
����2����֪1.0mol•L-1NaHSO3��Һ��pHΪ3.5��������ˮ������ҺpHѸ�ٽ��ͣ���ҺpH���͵�ԭ����HSO3-+Cl2+H2O=3H++SO42-+2Cl-�������ӷ���ʽ��ʾ����
��3���ڳ��³�ѹ���������£�N2�ڴ�����TiO2��������H2O��Ӧ������1molNH3��O2ʱ�������仯ֵΪ382.5kJ���ﵽƽ���˷�ӦNH3���������¶ȵ�ʵ���������±�����÷�Ӧ���Ȼ�ѧ����ʽΪ$\frac{1}{2}$N2��g��+$\frac{3}{2}$H2O��l��?NH3��g��+$\frac{3}{4}$O2��g����H=+382.5kJ/mol����2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol����
| T/K | 303 | 313 | 323 |
| NH3������/��10-1mol�� | 4.3 | 5.9 | 6.0 |
2NH4+��aq��+Mg��OH��2��s��?Mg2+��aq��+2NH3•H2O��aq��
д��������Ӧ��ƽ�ⳣ������ʽK=$\frac{c��M{g}^{2+}��•{c}^{2}��N{H}_{3}•{H}_{2}O��}{{c}^{2}��N{{H}_{4}}^{+}��}$
ij�о���ѧϰС��Ϊ̽��Mg2+��NH3•H2O��Ӧ�γɳ���������������������ʵ��
| ʵ��� | �����1mol/L��ˮ��0.1mol/L MgCl2��Һ��� | ���ɰ�ɫ���� |
| ʵ��� | �����0.1mol/L��ˮ��1mol/L MgCl2��Һ��� | ������ |
��5���������£���ѧ��ӦI-��aq��+ClO-��aq��=IO-��aq��+Cl-��aq���ķ�Ӧ���ʼŨ�ȡ���Һ�е����������ӳ�ʼŨ�ȼ���ʼ���ʼ�Ĺ�ϵ���±���ʾ��
| ʵ���� | I-�ij�ʼŨ�� ��mol•L-1�� | ClO-�ij�ʼŨ�� ��mol•L-1�� | OH-�ij�ʼŨ�� ��mol•L-1�� | ��ʼ����v ��mol•L-1•s-1�� |
| 1 | 2��10-3 | 1.5��10-3 | 1.00 | 1.8��10-4 |
| 2 | a | 1.5��10-3 | 1.00 | 3.6��10-4 |
| 3 | 2��10-3 | 3��10-3 | 2.00 | 1.8��10-4 |
| 4 | 4��10-3 | 3��10-3 | 1.00 | 7.2��10-4 |
�����ʵ��2��ʵ��4��Ŀ����̽��ClO-�Է�Ӧ���ʵ�Ӱ�죻
����ʵ����4������Ũ�Ȳ��䣬������Һ�����ֵ���ΪpH=13����Ӧ�ij�ʼ����v=7.2��10-4��
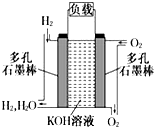 ����Ϊ�ı�δ�������ʮ���¿Ƽ�֮һ��ȼ�ϵ�ؾ�������Ⱦ������������Ч�ʵ��ص㣮��ͼΪ����ȼ�ϵ�صĽṹʾ��ͼ���������ҺΪKOH��Һ���缫����Ϊ���ɶ��ʯī�����������������ֱ��������ϵش�����������ͨ��ȼ�ϵ��ʱ������ڱպϻ�·�в��ϵز����������Իش��������⣺
����Ϊ�ı�δ�������ʮ���¿Ƽ�֮һ��ȼ�ϵ�ؾ�������Ⱦ������������Ч�ʵ��ص㣮��ͼΪ����ȼ�ϵ�صĽṹʾ��ͼ���������ҺΪKOH��Һ���缫����Ϊ���ɶ��ʯī�����������������ֱ��������ϵش�����������ͨ��ȼ�ϵ��ʱ������ڱպϻ�·�в��ϵز����������Իش��������⣺