题目内容
已知2A2(g)+B2(g)?2C3(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ.
(1)比较a b(填>、=、<)
(2)下表为不同温度下该反应的平衡常数.由此可推知,表中T1 T2(填“>”、“<”或“=”)
若在原来的容器中,只加入2mol C3,500℃时充分反应达平衡后,吸收热量c kJ,C3的浓度 (填>、=、<)w mol/L.
(3)在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是
A.4mol A2和2mol B2 B.4mol A2、2mol B2和2mol C2
C.4mol A2和4mol B2D.6mol A2和4mol B2
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 .
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂.
(1)比较a
(2)下表为不同温度下该反应的平衡常数.由此可推知,表中T1
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
(3)在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是
A.4mol A2和2mol B2 B.4mol A2、2mol B2和2mol C2
C.4mol A2和4mol B2D.6mol A2和4mol B2
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂.
考点:化学平衡常数的含义,化学平衡的影响因素
专题:化学平衡专题
分析:(1)根据可逆反应的特点分析;
(2)根据温度对平衡的影响来判断化学平衡常数的变化;正向投2molA2和1molB2,与逆向投2molC3,是等效平衡;
(3)由反应方程式可知生成2mol的C时放热a kJ,想得到2a kJ热量,则需生成4molC;由于反应是可逆反应,不可能完全进行到底,所以要得到4molC,A与B物质的量必须要多于4mol和2mol;
(4)为使该反应的反应速率增大,且平衡向正反应方向移动,依据影响化学反应速率和化学平衡的因素分析判断.
(2)根据温度对平衡的影响来判断化学平衡常数的变化;正向投2molA2和1molB2,与逆向投2molC3,是等效平衡;
(3)由反应方程式可知生成2mol的C时放热a kJ,想得到2a kJ热量,则需生成4molC;由于反应是可逆反应,不可能完全进行到底,所以要得到4molC,A与B物质的量必须要多于4mol和2mol;
(4)为使该反应的反应速率增大,且平衡向正反应方向移动,依据影响化学反应速率和化学平衡的因素分析判断.
解答:
解:(1)热化学方程式表达的意义为:当2mol A2和1mol B2完全反应时,放出热量为akJ,而加入2mol A2和1mol B2达到平衡时,可逆反应没有完全进行,即释放的热量小于完全反应释放的热量,即b<a,
故答案为:>;
(2)已知该反应为放热反应,升高温度,化学平衡向逆反应方向移动,生成物浓度减小,反应物浓度增大,K减小,所以K越大,则温度越低,所以T1<T2,正反投2molA2和1molB2,与逆向投2molC3,是等效平衡,所以反应达平衡后,C3浓度等于 w mol/L;
故答案为:<;=;
(3)由反应方程式可知生成2mol的C时放热a kJ,想得到2a kJ热量,则需生成4molC;由于反应是可逆反应,不可能完全进行到底,所以要得到4molC,A与B物质的量必须要多于4mol和 2mol,故D符合,B选项中既有正反应又有逆反应,最终放出的热量小于2akJ,
故答案为:D;
(4)已知2A(g)+B(g)?2 C(g),△H=-a kJ/mol(a>0),反应是气体体积减小的放热反应,依据平衡移动原理分析,反应的反应速率增大,且平衡向正反应方向移动;
A.及时分离出C气体,反应正向进行,但反应速率减小,故A不符合;
B.适当升高温度,加快反应速率,但平衡逆向进行,故B不符合;
C.增大B的浓度,平衡正向进行,反应速率增大,故C符合;
D.选择高效催化剂,增大反应速率,但不改变平衡,故D不符合;
故答案为:C.
故答案为:>;
(2)已知该反应为放热反应,升高温度,化学平衡向逆反应方向移动,生成物浓度减小,反应物浓度增大,K减小,所以K越大,则温度越低,所以T1<T2,正反投2molA2和1molB2,与逆向投2molC3,是等效平衡,所以反应达平衡后,C3浓度等于 w mol/L;
故答案为:<;=;
(3)由反应方程式可知生成2mol的C时放热a kJ,想得到2a kJ热量,则需生成4molC;由于反应是可逆反应,不可能完全进行到底,所以要得到4molC,A与B物质的量必须要多于4mol和 2mol,故D符合,B选项中既有正反应又有逆反应,最终放出的热量小于2akJ,
故答案为:D;
(4)已知2A(g)+B(g)?2 C(g),△H=-a kJ/mol(a>0),反应是气体体积减小的放热反应,依据平衡移动原理分析,反应的反应速率增大,且平衡向正反应方向移动;
A.及时分离出C气体,反应正向进行,但反应速率减小,故A不符合;
B.适当升高温度,加快反应速率,但平衡逆向进行,故B不符合;
C.增大B的浓度,平衡正向进行,反应速率增大,故C符合;
D.选择高效催化剂,增大反应速率,但不改变平衡,故D不符合;
故答案为:C.
点评:本题考查了等效平衡、影响平衡的因素、平衡常数等知识,题目综合性强,难度中等,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
刚玉(主要成分是Al2O3)是人造红宝石和蓝宝石的原料.现用废铝屑、废酸液和废碱液来生产刚玉.为达到最大生产效率,安排生产时,废铝屑分别与废酸液作用和废碱液作用的质量比为( )
| A、1:1 | B、1:2 |
| C、1:3 | D、3:1 |
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+═Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
| A、该装置可能是原电池,可用Cu、C作电极,电解质溶液是盐酸 |
| B、该装置可能是原电池,电解质溶液为硝酸 |
| C、该装置只能是电解池,金属铜为该电解池的阳极,K2SO4为电解质溶液 |
| D、该装置只能是电解池,金属铜为该电解池的阳极,稀H2SO4为电解质溶液 |
在下列各溶液中,一定能大量共存的离子组是( )
| A、强酸性溶液中:K+、S2-、ClO-、SO42- |
| B、含有0.1mol?L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
| C、室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
| D、加入Al能放出H2的溶液中::Na+、K+、CO32-、Cu2+ |
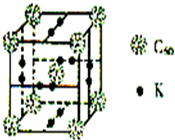 碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题:
碳、氢、氟、氮、硅等非金属元素与人类的生产生活息息相关.回答下列问题: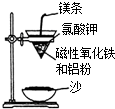 某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题:
某校高三同学高考前重做以下两个课本实验,请你回答实验过程中的相关问题: