题目内容
【题目】现有核电荷数小于18的元素A,其电离能数据如表所示[I1表示失去第1个电子的电离能,In(n=2,3,4,5,6,7,8,9,10,11)表示失去第n个电子的电离能,单位为eV]。
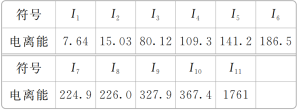
(1)外层电子离核越远,能量越高,电离能越______(填“大”或“小”);阳离子所带电荷数越多,在失去电子时,电离能越________(填“大”或“小”)。
(2)上述11个电子分属________个电子层。
(3)去掉11个电子后,该元素还有________个电子。
(4)该元素的最高价氧化物对应的水化物的化学式是________。
【答案】小 大 3 1 Mg(OH)2
【解析】
根据电离能I2与I3之间产生了突变,可知该原子最外层有2个电子,核电荷数小于18的元素,且已有11个电子,所以该元素为12号镁。
(1) 据图表可知外层电子离核越远,能量越高,越容易失去电子,所以电离能越小;阳离子电荷数越高,原子核对核外电子的引力越大,越难失去电子,电离能越大;
(2) 从表格能量大小可看出,前两个电子在一个能层,之后八个在一个能层,最后一个在一个能层,故分属3个电子层;
(3) 该元素为12号Mg,失去了11个电子后,该元素还有1个电子;
(4) Mg的最高价氧化物对应的水化物的化学式是Mg(OH)2。

练习册系列答案
相关题目