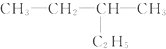题目内容
12.下面是某同学研究氯水漂白性的一个探究性实验片断.活动计录:【观察】氯气的颜色:黄绿色;氯水的颜色:呈黄绿色.
【结论】氯水中含有氯气分子.
【实验操作】用两根玻璃棒分别蘸取盐酸和氯水,各滴在两片蓝色石蕊试纸上.
【实验现象】滴有盐酸的试纸变红色,滴有氯水的试纸中间变白,外圈变红.
【分析与结论】氯水呈黄绿色,说明氯水中溶有氯气分子.滴有氯水的蓝色石蕊试纸外圈变红,说明氯水中有能使试纸变红的酸生成;中间变白,说明氯水中有能够使有色物质褪色的物质生成.
【问题与思考】氯气溶于水发生如下反应:Cl2+H2O═HCl+HClO,溶液中的水和盐酸都没有漂白作用,能够使有色物质褪色的物质是氯水中的氯气分子还是氯水中的次氯酸呢?还是二者都有漂白作用?
请你参照他已完成的部分实验活动记录,自己设计一个实验,证明到底是哪种物质有漂白作用.
【实验操作】将干燥的氯气分别通入装有干燥的红纸、潮湿的红纸的集气瓶.
【实验现象】干燥的红纸不变色,潮湿的红纸褪色.
【分析与结论】氯分子不具有漂白作用,次氯酸才能使有色物质褪色.
分析 【结论】根据氯气和氯水的颜色可以判断氯水中含有氯气分子;
【实验现象】盐酸显示酸性,能够使蓝色石蕊试纸变红;
【分析与结论】氯水呈黄绿色,说明氯水中溶有氯气分子;
【问题与思考】氯气与水反应生成氯化氢和次氯酸,据此写出反应的化学方程式;
根据Cl2+H2O═HCl+HClO,设计实验证明干燥的氯气、水、盐酸都没有漂白性,而氯水有漂白性,就可推知氯水的漂白性实质为氯气和水反应生成的次氯酸的漂白性,据此进行设计实验方案.
解答 解:【结论】氯气的颜色为黄绿色;氯水的颜色也呈黄绿色,说明氯水中含有氯气分子,
故答案为:氯气;
【实验现象】盐酸能够使蓝色石蕊试纸变红,则滴有盐酸的试纸变红色,
故答案为:红;
【分析与结论】氯水呈黄绿色,说明氯水中溶有氯气分子,
故答案为:氯气;
【问题与思考】氯气与水反应生成氯化氢和次氯酸,反应方程式为:Cl2+H2O═HCl+HClO,
故答案为:Cl2+H2O═HCl+HClO;
根据Cl2+H2O═HCl+HClO,设计实验证明干燥的氯气、水、盐酸都没有漂白性,而氯水有漂白性,就可推知氯水的漂白性实质为氯气和水反应生成的次氯酸的漂白性;收集干燥的氯气用有色纸条设计实验进行检验,湿润的有色纸条遇到干燥氯气会褪色,干燥有色纸条遇到干燥氯气不褪色证明,据此可设计如下实验方案:
【实验操作】收集一集气瓶干燥的氯气,用镊子夹取一片一端湿润的有色纸条,伸入盛有干燥氯气的集气瓶中,
【实验现象】有色纸条湿润的一端褪色,另一端无明显变化
【分析与结论】干燥的有色纸条不褪色,证明氯气本身无漂白作用.又知水和盐酸都没有漂白作用,容易推知:湿润的有色纸条褪色,是因为氯气溶于水发生反应Cl2+H2O═HCl+HClO,溶液中的次氯酸具有漂白性;
故答案为:[操作]将干燥的氯气分别通入装有干燥的红纸、潮湿的红纸的集气瓶;[现象]干燥的红纸不变色,潮湿的红纸褪色;[结论]氯分子不具有漂白作用,次氯酸才能使有色物质褪色.
点评 本题考查了物质性质验证实验的设计,侧重考查氯气、次氯酸性质比较分析判断,题目难度中等,注意掌握氯气的化学性质,明确次氯酸具有漂白性,氯气无漂白性.

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案| A. | 只有① | B. | 只有② | C. | ①②③的混合物 | D. | ①②③④的混合物 |
①a、c、e皆能与稀硫酸反应放出气体;
②b与d的硝酸盐反应,置换出单质d;
③c与强碱反应放出气体;
④c、e在冷浓硫酸中发生钝化.由此可判断a、b、c、d、e依次为( )
| A. | Fe Cu Al Ag Mg | B. | Al Cu Mg Ag Fe | ||
| C. | Mg Cu Al Ag Fe | D. | Mg Ag Al Cu Fe |
| A. | 正戊烷和正己烷 | B. | 苯和乙烷 | ||
| C. | 对二甲苯和2,2-二甲基丙烷 | D. | 甲苯和2-甲基丁烷 |
 翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅.
翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅.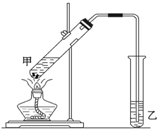 在实验室里用乙醇、冰醋酸和浓硫酸来制备一种有香味的物质,实验装置如图所示,请根据要求作答.
在实验室里用乙醇、冰醋酸和浓硫酸来制备一种有香味的物质,实验装置如图所示,请根据要求作答.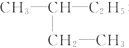 和
和
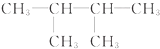 和
和