题目内容
【题目】某实验小组利用下图所示装置在实验室欲制备乙酸乙酯。
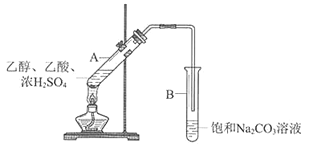
(1)B装置中,导管口略高于液面的目的是________________________
(2)为了改善反应过程中混合溶液变黑的现象,甲同学采用NaHSO4代替浓硫酸做催化剂(其他试剂及用量不变)来制备乙酸乙酯,NaHSO4可代替浓硫酸做催化剂的原因是__________________________________________________________
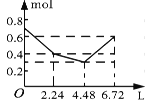
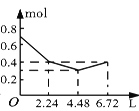
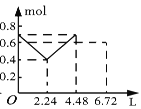
(3)下图是甲同学采用NaHSO4做催化剂,其他条件不变(其中乙酸用量为2 mL)不同质量的NaHSO4来制备乙酸乙酯的催化效果图,其中NaHSO4的质量为_______g时催化效果最好。

(4)乙同学实验时,在饱和NaCO3中滴加两滴酚酞,实验结束,取下试管B振荡,红色褪去。为探究褪色的原因,进行如下实验。
编号 | ① | ② | ③ |
实验 |
|
|
|
操作 | 充分振荡、静置 | 充分振荡、静置 | 充分振荡、静置、分液。取下层溶液,加入饱和Na2CO3溶液 |
现象 | 上层液体变薄,冒气泡,下层溶液红色褪去 | 上层液体不变薄,无气泡,下层溶液红色褪去 |
a试管①中产生气泡的原因是(用化学方程式解释)____________________________。
b对比实验①和②可得出的结论是___________________________________。
c针对实验②中现象,乙同学提出猜想:酚酞更易溶于乙酸乙酯。实验③中观察到__________________________________,证实乙的猜想正确。
【答案】防止倒吸 NaHSO4也可以电离出H+和SO42- 0.1 a. 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O b.下层溶液红色褪去的原因与乙酸无关 C. 溶液不变红或无明显现象
【解析】
(1)B装置中,导管口略高于液面的目的是防止倒吸。
(2)浓硫酸做催化剂,浓硫酸利用的浓硫酸的酸性和吸水性,采用NaHSO4代替浓硫酸做催化剂,是因为NaHSO4也可以电离出H+和SO42-。
(3)从图中乙酸乙酯的高度最高值读出;
(4)a、试管①中有末反应的醋酸,碳酸钠被反应消耗,酚酞红色褪去。
b、乙酸乙酯能将酚酞从碳酸钠溶液中萃取出去。
c、乙酸乙酯能将酚酞从水中萃取出去,在水层中再加碳酸钠,没有酚酞与之作用。
(1)B装置中,导管口略高于液面的目的是防止倒吸。
(2)浓硫酸具有脱水性,为了改善反应过程中混合溶液变黑的现象,用NaHSO4代替浓硫酸做催化剂(其他试剂及用量不变)来制备乙酸乙酯,浓硫酸作催化剂利用的浓硫酸的酸性和吸水性,采用NaHSO4代替浓硫酸做催化剂,是因为NaHSO4也可以电离出H+和SO42-。
(3)从图中乙酸乙酯的高度最高值读出:其中NaHSO4的质量为0.1g时催化效果最好。;
(4)a、试管①中有末反应的醋酸,产生气泡的原因是(用化学方程式解释)2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O,碳酸钠被反应消耗,酚酞红色褪去。
b、对比实验①和②可得出的结论是下层溶液红色褪去的原因与乙酸无关,乙酸乙酯能将酚酞从碳酸钠溶液中萃取出去。
c、针对实验②中现象,乙同学提出猜想:酚酞更易溶于乙酸乙酯。实验③中观察到溶液不变红或无明显现象,证实乙的猜想正确。乙酸乙酯能将酚酞从水中萃取出去,在水层中再加碳酸钠,没有酚酞与之作用。

【题目】下列说法是否正确
(1) | (2) | (3) | (4) |
___ | ___ | ___ | ___ |
(1)22.4LO2中一定含有6.02×1023个氧分子
(2)将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L
(3)18gH2O在标准状况下的体积是22.4L
(4)在标准状况时,20mLNH3与60mLO2所含的分子个数比为1:3
【题目】几种短周期元素的原子半径及主要化合价如表:
元素代号 | X | Y | Z | W |
原子半径 | 160 | 143 | 70 | 66 |
主要化合价 |
|
|
|
|
下列叙述正确的是
A. X的电负性大于Y的电负性
B. W的氢化物比同族其它元素的氢化物稳定,是因为W的氢化物中存在氢键
C. Y的最高价氧化物对应的水化物能溶于稀硫酸和稀氨水
D. W的非金属性比Y强