题目内容
6.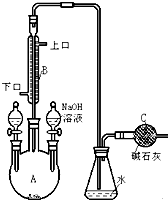 制备溴苯的实验装置如图所示,回答下列问题:
制备溴苯的实验装置如图所示,回答下列问题:(1)装在左侧分液漏斗中的药品是苯、液溴.
(2)反应方程式C6H6+Br2$\stackrel{催化剂}{→}$C6H5Br+HBr.
(3)将左侧分液漏斗的旋纽打开后,在A中可观察到的现象是瓶内开始时液面有轻微跳动,慢慢剧烈起来(微沸),瓶中出现红棕色气体.
(4)冷凝管B有上、下两口,冷却水应从下口进入.
(5)右侧分液漏斗中的物质在什么时候加入A中?反应结束时.其作用是除去未反应的溴和烧瓶中的HBr.
(6)要证明该反应是取代反应,最方便的实验方法是反应后,取锥形瓶中液体,滴加AgNO3溶液,若产生浅黄色沉淀则得证.
分析 (1)装在左侧分液漏斗中的药品是反应物苯和液溴;
(2)苯与液溴反应生成溴苯的反应方程式;
(3)左侧分液漏斗的旋纽打开后,溴与苯发生反应,该反应为放热反应;
(4)冷却水应从下口流入,上口流出,流速较慢,可达到更好的冷凝效果;
(5)制备溴苯完成后,加入氢氧化钠溶液除掉过量的Br2和生成的溴化氢;
(6)根据溴离子与硝酸银反应生成溴化银检验
解答 解:(1)装在左侧分液漏斗中的药品是反应物苯和液溴,
故答案为:苯、液溴;
(2)苯与液溴反应的化学方程式为:C6H6+Br2$\stackrel{催化剂}{→}$C6H5Br+HBr,
故答案为:C6H6+Br2$\stackrel{催化剂}{→}$C6H5Br+HBr;
(3)左侧分液漏斗的旋纽打开后,溴与苯发生反应,该反应为放热反应,所以可以看到三颈烧瓶内开始时液面有轻微跳动,慢慢剧烈起来(微沸),瓶中出现红棕色气体,
故答案为:瓶内开始时液面有轻微跳动,慢慢剧烈起来(微沸),瓶中出现红棕色气体;
(4)冷却水应从下口流入,上口流出,流速较慢,可达到更好的冷凝效果,
故答案为:下;
(5)Br2是制备溴苯的反应物,制备溴苯完成后,加入氢氧化钠溶液除掉过量的Br2和生成的溴化氢,
故答案为:反应结束时;除去未反应的溴和烧瓶中的HBr;
(6)可以根据溴离子与硝酸银反应生成溴化银检验,
故答案为:反应后,取锥形瓶中液体,滴加AgNO3溶液,若产生浅黄色沉淀则得证.
点评 本题考查了溴苯的制备,注重了基础知识考查,根据所学知识完成即可,本题难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
7.下列物质既能跟浓H2SO4反应,又能与烧碱反应的是( )
①MgCl2 ②NaHCO3 ③(NH4)2S ④Al(OH)3.
①MgCl2 ②NaHCO3 ③(NH4)2S ④Al(OH)3.
| A. | 只有④ | B. | 除①外 | C. | 除①③ | D. | 全部都可以 |
18.二氧化锰是一次电池制造的基本材料.工业上以软锰矿为原料制备高纯二氧化锰的流程如下:
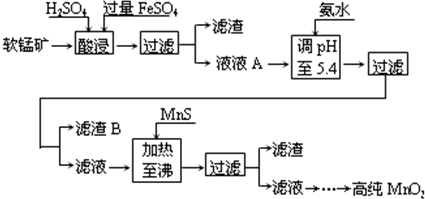
某软锰矿的主要成分为MnO2,还含有Si(16.72%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O.
(2)滤渣B的主要成分有Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.

某软锰矿的主要成分为MnO2,还含有Si(16.72%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)滤渣B的主要成分有Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.
16.下列说法中不正确的是( )
| A. | σ键是原子轨道以“头碰头”的方式相互重叠 | |
| B. | 共价化合物分子的键能越大,键长越长,则分子越稳定 | |
| C. | 2个原子形成多个共价键中,只有一个σ键,而π键可以是一个或多个 | |
| D. | 形成共价键时键与键重叠程度越大,体系能量越底,键越稳定 |
 .
.