题目内容
15.在恒温、恒容的密闭容器中加人一定量的PCl3和Cl2发生反应:PCl3(g)+Cl2(g)$\stackrel{催化剂}{?}$PCl3(g)△H<0,下列示意图正确且能说明反应在t1时刻已达到最大限度的是( )| A. |  | B. |  | C. | 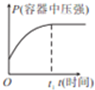 | D. |  |
分析 反应到达平衡状态时,正逆反应速率相等,平衡时各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,由此进行判断.
解答 解:A、t1时刻PCl3(g)和PCl3(g)的物质的量相等,并且反应物还在减小,生成物还在增大,则不能说明达到最大限度,故A错误;
B、平衡常数仅与温度有关,温度一定平衡常数始终不会改变,所以不能据此判断反应是否达到平衡状态,故B错误;
C、该反应是一个反应前后气体体积减小的可逆反应,随着反应的进行,压强应该减小,而不是增大,故C错误;
D、t1时刻,逆反应速率不在变化,则说明正逆反应速率相等,反应到达平衡状态,故D正确.
故选D.
点评 本题考查了图象的判断以及平衡状态的判断,注意把握化学平衡状态判断的角度,特别是正逆反应速率的关系,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.现有部分短周期元素的性质与原子(或分子)结构如下表:
(1)W在周期表中位于第二周期第VIA主族;元素Y与元素Z相比,金属性较强的是Na(用元素符号表示).下列表述中能证明这一事实的是cd(填序号).
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.单质Y能与冷水剧烈反应而Z不能
d.最高价氧化物对应的水化物碱性YOH强于Z(OH)2
(2)上述元素可形成含有共价键的二元离子化合物(包含两种不同元素的离子化合物),该化合物的化学式为Na2O2,该物质中阴阳离子个数比为1:2.
(3)W、X的氢化物H2W2、X2H4在一定条件下反应可得到一种在空气中体积分数最大的单质与常温下为液体的物质,写出该反应的化学方程式:2H2O2+N2H4=N2+4H2O.
| 元素符号 | W | X | Y | Z |
| 原子消息 | 海水中质量分数最高的元素 | 非金属性强而单质(X2)很稳定 | M层比K层少1个电子 | 第三周期元素的简单离子中半径最小 |
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.单质Y能与冷水剧烈反应而Z不能
d.最高价氧化物对应的水化物碱性YOH强于Z(OH)2
(2)上述元素可形成含有共价键的二元离子化合物(包含两种不同元素的离子化合物),该化合物的化学式为Na2O2,该物质中阴阳离子个数比为1:2.
(3)W、X的氢化物H2W2、X2H4在一定条件下反应可得到一种在空气中体积分数最大的单质与常温下为液体的物质,写出该反应的化学方程式:2H2O2+N2H4=N2+4H2O.
10.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温下,16gO2含有16NA个电子 | |
| B. | 一个CO分子、CO2分子的质量分子分别是ag、bg,则氧原子的相对原子质量是NA(b-a) | |
| C. | 0.1mol.L-1CH3COOH溶液中含有CH3COOH-的数目为0.1NA | |
| D. | 将2molSO2和10molO2充入一密闭容器中充分反应后,生成SO3的分子数为2NA |
20.下列溶液pH一定等于1的是( )
| A. | 25℃1L的0.1mol•L-1H2SO4溶液 | |
| B. | T℃1L 0.2mol•L-1H2SO4溶液中加入1L 0.2mol•L-1NaOH溶液后得到的2L溶液 | |
| C. | 25℃a mol•L-1NaHSO4溶液[已知50ml amol•L-1Ba(OH)2溶液与100mL amol•L-1NaHSO4溶液混合后pH=7] | |
| D. | T℃c(OH-)=10-13mol•L-1的某盐溶液 |
7.将2.7g铝溶解于100mL3mol/LNaOH溶液中,然后向所得溶液中加入400mL,1mol/L的盐酸,最后可得沉淀的质量是( )
| A. | 2.7g | B. | 5.2g | C. | 7.8g | D. | 10g |
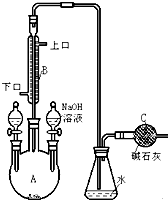 制备溴苯的实验装置如图所示,回答下列问题:
制备溴苯的实验装置如图所示,回答下列问题: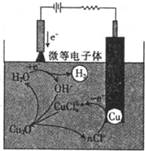 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题: .
.