题目内容
【题目】已知十种物质:①H2O ②空气 ③ Mg ④ CaO ⑤H2SO4 ⑥氢氧化钡⑦饱和FeCl3溶液 ⑧氨水 ⑨HNO3 ⑩胆矾,根据上述提供的物质,回答下列问题:
(1)属于混合物的是__________ (填序号,下同),属于电解质的是__________ 。
(2)上述物质中__________与__________在水溶液中可发生反应,且离子方程式为H++OH-=H2O。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________,反应的离子方程式为__________;证明有Fe(OH)3胶体生成的实验操作及现象是__________
(4)实验室配制900mL 0.1mol/L硫酸铜溶液,需要称取的溶质(从上述物质中选取)的质量为__________g,从配制好的溶液中取出300mL,其中含有SO42-的数目为__________(设
NA为阿伏加德罗常数的值)。
【答案】②⑦⑧ ①④⑤⑥⑨⑩ ⑥ ⑨ ①⑦ Fe3++3H2O ![]() Fe(OH)3(胶体)+3H+ 用激光笔照射,侧面若有一条明亮的光路,则证明有胶体生成 25.0 0.03NA
Fe(OH)3(胶体)+3H+ 用激光笔照射,侧面若有一条明亮的光路,则证明有胶体生成 25.0 0.03NA
【解析】
(1)①H2O是纯净物,属于电解质;②空气是混合物,不是电解质;③ Mg属于单质,能导电,但不是电解质也不是非电解质;④ CaO是纯净物,属于电解质;⑤H2SO4 属于纯净物,属于电解质;⑥氢氧化钡是纯净物,属于电解质;⑦饱和FeCl3溶液属于混合物,不是电解质;⑧氨水是混合物,不是电解质;⑨HNO3是纯净物,属于电解质;⑩胆矾是纯净物,属于电解质;
(2)酸碱中和反应的实质是H++OH-=H2O;
(3)实验室制备Fe(OH)3胶体的方法是:将饱和的FeCl3溶液滴入沸水中,加热至溶液变为红褐色,得到的即为Fe(OH)3胶体;反应的方程式为:Fe3++3H2O ![]() Fe(OH)3(胶体)+3H+;利用丁达尔效应检验胶体;
Fe(OH)3(胶体)+3H+;利用丁达尔效应检验胶体;
(4)实验室制备硫酸铜溶液,可选择胆矾(⑩),实验室没有900ml的容量瓶,因此选择1000ml的容量瓶,根据公式m=cVM计算需要溶质的质量并进行SO42-的数目的计算。
(1)根据分析可知:②⑦⑧属于混合物;①④⑤⑥⑨⑩时电解质;
(2)H++OH-=H2O表示的是酸碱发生中和生成可溶性盐的反应,即氢氧化钡(⑥)和硝酸(⑨)反应;
(3)由分析可知,实验室制备少量Fe(OH)3胶体所用的物质有饱和的FeCl3溶液(⑦)和水(①);反应的方程式为:Fe3++3H2O ![]() Fe(OH)3(胶体)+3H+;利用丁达尔效应检验胶体,即用激光笔照射,侧面若有一条明亮的光路,则证明有胶体生成;
Fe(OH)3(胶体)+3H+;利用丁达尔效应检验胶体,即用激光笔照射,侧面若有一条明亮的光路,则证明有胶体生成;
(4)需要称取胆矾的质量m=cVM= 0.1mol/L×1L×250g/mol=25.0g;从1000ml 0.1mol/L的硫酸铜溶液中取出300ml,溶液中SO42-的物质的量为0.3L×0.1mol/L=0.03mol,因此含有SO42-的数目为0.03NA。

【题目】叠氮化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。下面是工业水合肼法制备叠氮化钠的工艺流程:

查阅资料:
①水合肼(N2H4·H2O)有毒且不稳定,具有强还原性和强碱性。
②有关物质的物理性质如下表:
物质 | 熔点℃ | 沸点℃ | 溶解性 |
CH3OH | -97 | 64.7 | 与水互溶 |
水合肼(N2H4·H2O) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚 |
亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
叠氮化钠(NaN3) | 275 (410易分解) | —— | 易溶于水,微溶于醇, 不溶于乙醚 |
(1)合成水合肼。
实验室合成水合肼装置如图所示。NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应可以制得水合肼。
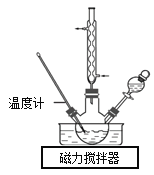
①制取N2H4·H2O的离子方程式为_________。
②实验中通过分液漏斗滴加的溶液是_________,理由是_________。
(2)水合肼法制备叠氮化钠。
①实验室模拟工艺流程步骤Ⅰ制备叠氮化钠的反应原理为:N2H4·H2O(aq)+CH3ONO(g)+NaOH(aq)=NaN3(aq)+CH3OH(aq)+3H2O(l) △H﹤0, 研究表明该反应在20℃左右反应的选择性和转化率最高,实验时可以采取的措施是_________。
②步骤Ⅱ回收CH3OH的实验操作名称为________。
③请设计由B溶液获得叠氮化钠(NaN3)产品的实验方案:_________[实验中可供选择的试剂有:乙醇、乙醚;除常用仪器外须使用的仪器有:布氏漏斗、真空干燥箱]。