题目内容
10.将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置(以下均假设反应过程溶液的体积不变).(1)铁片上的电极反应式为Fe-2e-=Fe2+;
(2)若2min后测得铁片和铜片之间的质量差为1.2g,计算:导线中流过的电子的物质的量为0.02mol;
(3)某温度时,在体积为5L的密闭容器中加入2mol Fe(s)与1mol H2O (g),t1秒后,H2的物质的量为0.20mol,到t2秒时恰好达到平衡,此时H2的物质的量为0.35mol.
①若继续加入2mol Fe(s),则逆反应速率不变(填“增大”、“减小”或“不变”),继续通入1mol H2O(g),则正反应的速率增大.
②该反应的逆反应速率随时间变化的关系如图2.t1时改变了某种条件,改变的条件可能是加入催化剂或升高温度、增大气体反应物浓度(填写2项).

分析 (1)铁比铜活泼,为原电池的负极,发生氧化反应;
(2)铜为正极,发生还原反应,电极方程式为Cu2++2e-=Cu,结合电极方程式解答该题;
(3)①根据固体不影响反应速率和化学平衡判断;根据反应物浓度增大,正反应速率增大,生成物物质的量增大完成;
②根据t1时逆反应速率变化判断改变的条件.
解答 解:(1)铁比铜活泼,为原电池的负极,发生氧化反应,电极方程式为Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+;
(2)设转移xmol电子,则消耗0.5xmolFe,析出0.5xmolCu,则有0.5x×(64+56)=1.2,x=0.02,故答案为:0.02;
(3)①在固体有剩余的情况下,增加或减少固体的质量,对反应速率以及限度均无影响;加入水蒸气,反应物浓度增大,正反应速率增大,氢气的物质的量增大,
故答案为:不变;增大;
②t1时反应未达到平衡,改变条件后逆反应速率突然增大,且继续增大,可知为加入催化剂或升高温度或增大气体反应物浓度,
故答案为:加入催化剂或升高温度;增大气体反应物浓度.
点评 本题考查原电池知识、化学反应速率的计算、化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握原电池的工作原理,把握电极方程式的书写.

练习册系列答案
相关题目
20.下列关于镁和钠及其合金的比较结论正确的是( )
| A. | 铝镁合金的硬度较大,钠钾合金的硬度较小 | |
| B. | 因为钠的金属性比镁要强,所以钠的熔点比镁要高 | |
| C. | 镁能置换硫酸铜中的铜,钠也能置换硫酸铜中的铜 | |
| D. | 在空气中都能被点燃,生成的产物都是氧化物,无过氧化物 |
18.下列说法正确的是( )
| A. | 淀粉、纤维素、油脂、蛋白质都属于高分子化合物 | |
| B. | 笔和墨的原料中都存在蛋白质 | |
| C. | 纸的主要成分属于糖类 | |
| D. | 将新鲜的土豆切开,一段时间后可观察到切面变蓝,说明土豆中含有Cu2+ |
5.分子式为C7H16O的饱和一元醇发生消去反应时,可以得到两种单烯烃,则该醇的结构简式是( )
| A. | 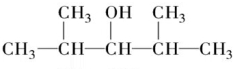 | B. | 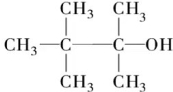 | ||
| C. |  | D. | CH3(CH2)5CH2OH |
2.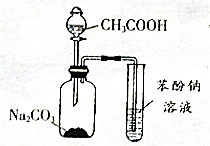 下列关于如图实验的说法错误的是( )
下列关于如图实验的说法错误的是( )
 下列关于如图实验的说法错误的是( )
下列关于如图实验的说法错误的是( )| A. | 集气瓶中的离子方程式是:2CH3COOH+CO32-→2CH3COO-+H2O+CO2 ↑ | |
| B. | 少量的CO2通入苯酚钠中生成苯酚和碳酸钠 | |
| C. | 醋酸和苯酚钠发生反应 | |
| D. | 该装置和相关实验现象能推出酸性强弱顺序为:CH3COOH>H2CO3 >C6H5OH |
19.酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
回答下列问题:
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为:2MnO2+Zn+2H+=2MnOOH+Zn2+.
(2)维持电流强度为0.5A,电池工作五分钟,理论消耗锌0.05g.(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,两者可以通过加热浓缩冷却结晶分离回收,滤渣的主要成分是MnO2、碳粉和MnOOH,欲从中得到较纯的MnO2,最简便的方法是空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰.
(4)用废电池的锌皮制作ZnSO4•7H2O的过程中,需除去铁皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2,溶解,铁变为Fe3+加碱调节pH为2.7时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全).继续加碱调节pH为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2的后果是Zn2+和Fe2+分离不开,原因是Zn(OH)2、Fe(OH)2的Ksp相近.
溶解度/(g/100g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为:2MnO2+Zn+2H+=2MnOOH+Zn2+.
(2)维持电流强度为0.5A,电池工作五分钟,理论消耗锌0.05g.(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,两者可以通过加热浓缩冷却结晶分离回收,滤渣的主要成分是MnO2、碳粉和MnOOH,欲从中得到较纯的MnO2,最简便的方法是空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰.
(4)用废电池的锌皮制作ZnSO4•7H2O的过程中,需除去铁皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2,溶解,铁变为Fe3+加碱调节pH为2.7时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全).继续加碱调节pH为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2的后果是Zn2+和Fe2+分离不开,原因是Zn(OH)2、Fe(OH)2的Ksp相近.
15.下列说法正确的是( )
| A. | 有些活泼金属,如铝可作还原剂法的还原剂 | |
| B. | 用电解NaCl溶液的方法来冶炼金属钠 | |
| C. | 可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 | |
| D. | 水煤气是通过煤的液化得到的气体燃料 |