题目内容
【题目】已知:①H2(g)+ ![]() O2(g)=H2O(g);ΔH1= akJ·mol-1
O2(g)=H2O(g);ΔH1= akJ·mol-1
②2H2(g)+O2(g) = 2H2O(g);ΔH2= b kJ·mol-1 ③ H2(g)+ ![]() O2(g)=H2O(l);ΔH3= c kJ·mol-1
O2(g)=H2O(l);ΔH3= c kJ·mol-1
④2H2(g)+O2(g) = 2H2O(l);ΔH4= d kJ·mol-1,下列关系式中正确的是( )
A.2a=b<0B.b>d>0C.a<c<0D.2c=d>0
【答案】A
【解析】
四个反应均为放热反应,即a、b、c、d均小于0,根据物质的状态及计量数比较a、b、c、d之间的关系和大小。
A. 反应①和②所有物质聚集状态相同,且反应②的计量数是反应①的2倍,则2a=b,所有反应均为放热反应,即a、b、c、d均小于0,因此2a=b<0,A项正确;
B. 四个反应均为放热反应,即a、b、c、d均小于0,B项错误;
C. 反应①和③对比,H2O的状态不同,从气态变为液态要放出热量,因此反应③放出的热量更多,那么c < a <0,C项错误;
D. 反应③和④所有物质聚集状态相同,且反应④的计量数是反应③的2倍,则2c=d,所有反应均为放热反应,即a、b、c、d均小于0,因此2c=d <0,D项错误;
答案选A。

【题目】甲醇既是基本有机化工原料,又可作为燃料用于替代矿物燃料。
(1)工业上合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
平衡常数K | 2.041 | 0.270 | 0.012 |
由表中数据判断该反应为 ________反应(填“吸热”或“放热”)。 某温度下,将2 molCO和6 molH2充入2 L的密闭容器中充分反应,达到平衡后,测得c(CO)=0.2 mol/L,则CO的转化率为______,此时的温度为______(从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2kJ/mol
③H2O(g)=H2O(l) ΔH3kJ/mol
则反应CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH= _____________ kJ/mol(用ΔH1、ΔH2、ΔH3表示)。
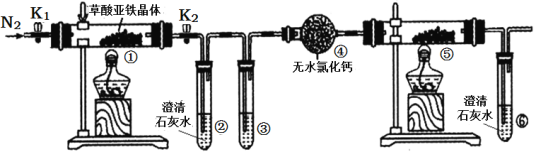
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法:

①N电极的电极反应式为 ___________________________________。
②请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:
Cr2O72 + ______ Fe2+ + ______ = ______ Cr3+ + ______ Fe3+ + ______
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×105 mol/L时,Cr3+沉淀完全,此时溶液的pH=______。(已知:Ksp=6.4×1031,lg2=0.3)
【题目】下列实验能达到实验目的是( )
序号 | 实验内容 | 实验目的 |
A | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向FeCl3+3KSCN | 说明增加生成物浓度,平衡逆向移动 |
C | 向盛有AgCl悬浊液的试管中滴加0.1mol·L-1NaI溶液,浊液变黄 | 证明相同温度下, KSP(AgCl)>KSP(AgI) |
D | 酸式滴定管中硫酸液面在20.00mL,将滴定管中液体全部放出 | 量取20.00mL硫酸溶液 |
A.AB.BC.CD.D