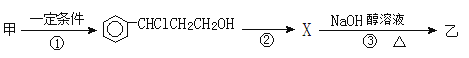题目内容
【题目】甲醇既是基本有机化工原料,又可作为燃料用于替代矿物燃料。
(1)工业上合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
CH3OH(g) ΔH。下表所列数据是该反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
平衡常数K | 2.041 | 0.270 | 0.012 |
由表中数据判断该反应为 ________反应(填“吸热”或“放热”)。 某温度下,将2 molCO和6 molH2充入2 L的密闭容器中充分反应,达到平衡后,测得c(CO)=0.2 mol/L,则CO的转化率为______,此时的温度为______(从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2kJ/mol
③H2O(g)=H2O(l) ΔH3kJ/mol
则反应CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH= _____________ kJ/mol(用ΔH1、ΔH2、ΔH3表示)。
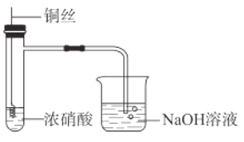
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法:

①N电极的电极反应式为 ___________________________________。
②请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:
Cr2O72 + ______ Fe2+ + ______ = ______ Cr3+ + ______ Fe3+ + ______
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×105 mol/L时,Cr3+沉淀完全,此时溶液的pH=______。(已知:Ksp=6.4×1031,lg2=0.3)
【答案】放热 80% 250℃ ![]() 或
或![]() (ΔH1-ΔH2)+2ΔH3 O2+4e+4H+=2H2O 6 14H+ 2 6 7H2O 5.6
(ΔH1-ΔH2)+2ΔH3 O2+4e+4H+=2H2O 6 14H+ 2 6 7H2O 5.6
【解析】
(1)由表中数据可知,随温度升高平衡常数减小,说明升高温度平衡逆向移动,则正反应为放热反应;
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始浓度(mol/L): 1 3 0
变化浓度(mol/L): 0.8 1.6 0.8
平衡浓度(mol/L): 0.2 1.4 0.8
由此计算CO转化率和此温度下平衡常数,进而判断温度;
(2)利用盖斯定律构造目标热化学方程式并求焓变;
(3)①氢离子由质子交换膜由M电极区移向N电极区,则M为负极、N为正极,负极上发生氧化反应,甲醇失去电子,生成二氧化碳与氢离子,正极发生还原反应,氧气获得电子,与通过质子交换膜的氢离子结合为水;
②电解池溶液里Cr2O72-转化为Cr3+,化合价降低共6价,左侧Fe电极为阳极,Fe失去电子生成Fe2+,酸性条件Fe2+将Cr2O72-还原为Cr3+,自身被氧化为Fe3+,化合价升高共1价,化合价升降最小公倍数为6,则Cr2O72-的系数为1,Fe2+的系数为6,再结合电荷守恒、原子守恒配平方程式;
(4)Ksp=c(Cr3+)×c3(OH-)=6.4×1031计算c(OH-),根据KW=c(H+)×c(OH-)计算溶液中c(H+),再根据pH=-lgc(H+)计算。
(1)由表中数据可知,随温度升高平衡常数减小,说明升高温度平衡逆向移动,则正反应为放热反应,故△H<0,某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始浓度(mol/L): 1 3 0
变化浓度(mol/L): 0.8 1.6 0.8
平衡浓度(mol/L): 0.2 1.4 0.8
CO转化率=![]() ×100%=80%,平衡常数K=
×100%=80%,平衡常数K=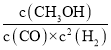 =
=![]() =2.041,故温度为250℃,
=2.041,故温度为250℃,
故答案为:放热;80%;250℃;
(2)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2kJ/mol
③H2O(g)=H2O(l) ΔH3kJ/mol
根据盖斯定律![]() (①②+4×③)可得:CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=
(①②+4×③)可得:CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H= ![]() 或
或![]() (ΔH1-ΔH2)+2ΔH3;
(ΔH1-ΔH2)+2ΔH3;
(3)①氢离子由质子交换膜由M电极区移向N电极区,则M为负极、N为正极,负极上发生氧化反应,甲醇失去电子,生成二氧化碳与氢离子,负极电极反应式为:CH3OH6e+H2O=6H++CO2↑,正极发生还原反应,氧气获得电子,与通过质子交换膜的氢离子结合为水,正极电极反应式为:O2+4e+4H+=2H2O,
故答案为:O2+4e+4H+=2H2O;
②电解池溶液里Cr2O72-转化为Cr3+,化合价降低共6价,左侧Fe电极为阳极,Fe失去电子生成Fe2+,酸性条件Fe2+将Cr2O72-还原为Cr3+,自身被氧化为Fe3+,化合价升高共1价,化合价升降最小公倍数为6,则Cr2O72-的系数为1,Fe2+的系数为6,反应离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:6;14H+;2;6;7H2O;
(4)Ksp=c(Cr3+)×c3(OH)=6.4×10-31,c(Cr3+)=1×10-5mol·L1时,溶液中c(OH)=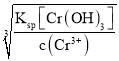 =
=![]() =4×10-9mol·L1,则c(H+)=
=4×10-9mol·L1,则c(H+)=![]() =
=![]() mol/L=2.5×10-6mol·L1,则pH=lg(2.5×10-6) =5.6。
mol/L=2.5×10-6mol·L1,则pH=lg(2.5×10-6) =5.6。

 小学课时特训系列答案
小学课时特训系列答案【题目】下列有关物质检验的实验操作、现象及结论均正确的是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO |
B | 向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定为SO2 |
D | 向某溶液中加入氢氧化钠溶液并加热,产生有刺激性气味气体,该气体能使湿润的蓝色石蕊试纸变红 | 该溶液中一定含有NH |
A.AB.BC.CD.D