题目内容
某稀溶液中含4molKNO3和2.5molH2SO4,向其中加入1.5molFe粉,充分反应后产生的NO气体在标准状况下的体积为( )
| A.36L | B.28L | C.22.4L | D.11.2L |
B
试题分析:硝酸钾和硫酸混合相当于是稀硝酸,所以与加入的铁粉反应实质是铁与稀硝酸的反应,所以应该用离子方程式解题。
Fe + 4H+ + NO3- =Fe3++NO↑+2H2O
1 : 4 : 1 1
1.5mol 5mol 4mol n
所以从比例关系来看,只有H+ 完全反应,所以n(NO)=1/4n(H+)=1.25mol,所以转化为标况下体积V(NO)=28L,故选B。

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
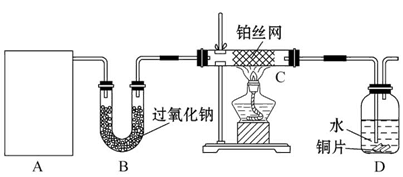
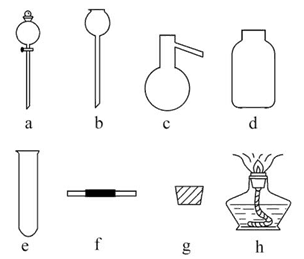


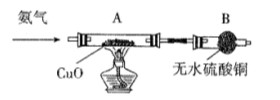
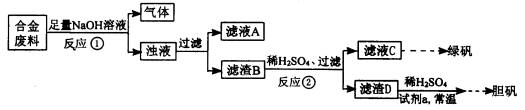
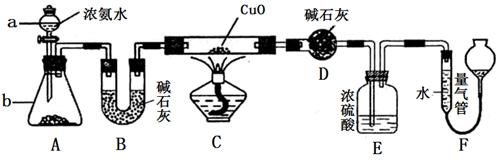
 Cu(NO3)2
Cu(NO3)2 Cu(NO3)2
Cu(NO3)2 Cu(NO3)2
Cu(NO3)2 CuO
CuO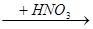 Cu(NO3)2
Cu(NO3)2