题目内容
由铜制备硝酸铜,考虑到生产成本和减少污染,下列最合理的方法是( )
A.Cu Cu(NO3)2 Cu(NO3)2 | B.Cu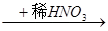 Cu(NO3)2 Cu(NO3)2 |
C.Cu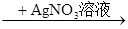 Cu(NO3)2 Cu(NO3)2 | D.Cu  CuO CuO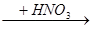 Cu(NO3)2 Cu(NO3)2 |
D
试题分析:AB、有毒气体生成,故错;C、成本有点高,故错。故选D。
点评:本题考查了学生根据所学的知识来判断如何从环保和经济的角度制取硝酸铜,培养了大家的环保理念,训练了学生对实验方案的选择能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

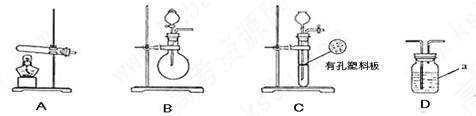
 .氧化铜反应后剩余固体的质量为
.氧化铜反应后剩余固体的质量为 .生成氮气在标准状况下的体积
.生成氮气在标准状况下的体积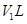 。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。
。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。 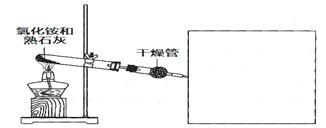
 2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
2N2+6H2O。和氢燃料相比有关数据见下表,据此判断正确的是
