题目内容
用大试管收集一试管NO2气体,倒扣在盛水的水槽里,试管内产生的现象为 ;再往试管里通入适量氧气,试管内又产生的现象为 。产生上述现象的原因是
试管内红棕色气体逐渐消失,水面上升至试管容积的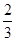 处 试管内又出现红棕色,接着红棕色消失,液面又上升。
处 试管内又出现红棕色,接着红棕色消失,液面又上升。
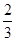 处 试管内又出现红棕色,接着红棕色消失,液面又上升。
处 试管内又出现红棕色,接着红棕色消失,液面又上升。 试题分析:用大试管收集一试管NO2气体,倒扣在盛水的水槽里,NO2与H2O反应:3NO2+H2O=2HNO3+NO,故颜色消失,液面上升至容积的
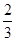 处;再充入O2时,发生反应2NO+O2=2NO2,故又出现了红棕色,NO2继续溶于水并与水反应,气体颜色又消失,液面又上升。2、NO的性质及反应现象的描述。
处;再充入O2时,发生反应2NO+O2=2NO2,故又出现了红棕色,NO2继续溶于水并与水反应,气体颜色又消失,液面又上升。2、NO的性质及反应现象的描述。 
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
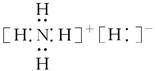

 2KNO2+O2↑
2KNO2+O2↑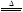 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑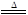 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑

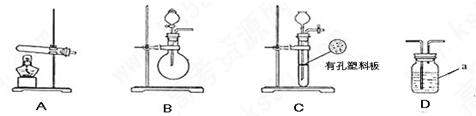
 .氧化铜反应后剩余固体的质量为
.氧化铜反应后剩余固体的质量为 .生成氮气在标准状况下的体积
.生成氮气在标准状况下的体积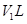 。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。
。乙小组测得洗气装置D前后的质量和生成氮气在标准状况下的体积。