题目内容
【题目】在下列溶液中Cl-的物质的量浓度最大的是
A. 0.5L 0.1mol/L的NaCl溶液 B. 100mL 0.2mol/L的MgCl2溶液
C. 1L 0.2mol/L的AlCl3溶液 D. 1L 0.3 mol/L盐酸溶液
【答案】C
【解析】
试题溶液中某一离子浓度的求法:该物质的浓度×该离子个数;A.C(Cl-)=0.1×1mol/L, BC(Cl-)=0.2×2mol/L;C.C(Cl-)=0.2×3mol/L ; D.C(Cl-)=0.3×1mol/L,综上,C最大;

【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则 =18
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
【题目】根据表中提供的数据(25 ℃),判断下列说法正确的是
化学式 | 电离常数 |
HClO | Ka=3.0×10-8 |
H2CO3 | Ka1=4.3×10-7 |
Ka2=5.6×10-11 |
A. 向氯水中加入硫酸,可增强杀菌效果
B. 温度升高,次氯酸的电离常数增大
C. 25 ℃时,ClO-的水解常数为3.0×10-6
D. 要提高氯水中HClO的浓度,可加入足量的Na2CO3固体
【题目】某同学设计实验制备2-羟基-4-苯基丁酸乙酯,反应原理、装置和数据如下:


相对分子质量 | 密度(g/cm3) | 沸点(℃) | 水溶性 | |
2-羟基-4-苯基丁酸 | 180 | 1.219 | 357 | 微溶 |
乙醇 | 46 | 0.789 | 78.4 | 易溶 |
2-羟基-4-苯基丁酸乙酯 | 208 | 1.075 | 212 | 难溶 |
实验步骤:
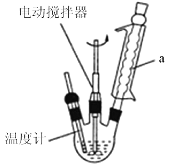
①如图1,在干燥的圆底烧瓶中加入20mL2-羟基-4-苯基丁酸、20mL无水乙醇和适量浓硫酸,再加入几粒沸石;
②加热至70℃左右保持恒温半小时;
③分离、提纯三颈瓶中的粗产品,得到有机粗产品;
④精制产品。
请回答下列问题:
(1)油水分离器的作用为__________。
(2)本实验采用水浴加热,因为温度过高会使产率_________ (填“增大”、“减小”或“不变”)。
(3)取三颈烧瓶中的混合物分别用水、饱和碳酸氢钠溶液和水洗涤。第二次水洗的目的是_________。
(4)在精制产品时,加入无水MgSO4的作用为____;然后过滤,再利用如图2装置进行蒸馏纯化,图2装置中的错误有_________。
(5)若按纠正后的操作进行蒸馏纯化,并收集212℃的馏分,得2-羟基-4-苯基丁酸乙酯约9.0g。则该实验的产率为_________。