题目内容
【题目】(1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示:
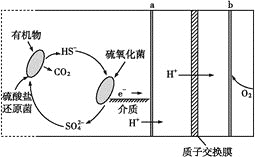
HS-在硫氧化菌作用下转化为SO![]() 的反应式是__。
的反应式是__。
(2)PbSO4热激活电池可用作火箭、导弹的工作电源,基本结构如图所示,其中作为电解质的无水LiCl—KCl受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。
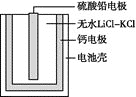
①放电过程中,Li+向__(填“负极”或“正极”)移动。
②负极反应式为__。
③电路中每转移0.2mol电子,理论上生成__gPb。
(3)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如图所示。
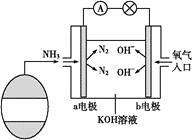
①a电极的电极反应式是__。
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因:__。
【答案】HS-+4H2O-8e-=SO![]() +9H+ 正极 Ca+2Cl--2e-=CaCl2 20.7 2NH3-6e-+6OH-=N2+6H2O 由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH
+9H+ 正极 Ca+2Cl--2e-=CaCl2 20.7 2NH3-6e-+6OH-=N2+6H2O 由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH
【解析】
3个问题都是原电池相关的问题,应用原电池原理解本题即可,假如是燃料电池,通入燃料的电极是负极、通入氧化剂的电极为正极,还原剂在原电池的负极发生氧化反应,书写电极反应式时要结合电解质,(1)中有质子交换膜,由图知负极上有氢离子生成、正极上有氢离子反应,(2)是无水盐环境,(3)在碱性电解质溶液中,电极上不能生成H+,据此回答;
(1)由微生物燃料电池的图可知,HS-在硫氧化菌作用下转化为SO![]() 的同时,还产生了氢离子,根据质量守恒和电荷守恒可写出相关的反应式为
的同时,还产生了氢离子,根据质量守恒和电荷守恒可写出相关的反应式为![]() ;
;
故答案为:![]() ;
;
(2)①电池放电过程中,阳离子向正极移动,Li+向正极移动,
答案为:正极;
②由电池总反应式可知,负极上是钙放电,产物为氯化钙,据此可知负极反应式为:Ca+2Cl--2e-=CaCl2
答案为:Ca+2Cl--2e-=CaCl2;
③由反应中的化合价变化可知,每生成1molPb,转移电子数为2mol,故电路中每转移0.2mol电子,理论上生成0.1molPb,质量为0.1mol ×207g/mol=20.7g;
答案为:20.7;
(3)①由电池工作图可知,氨气在a电极放电,产生氮气,碱性条件下,还产生水,故a电极的电极反应式是2NH3-6e-+6OH-=N2+6H2O;
答案为:2NH3-6e-+6OH-=N2+6H2O;
②一段时间后,需向装置中补充KOH的原因是由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH;
故答案为:由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH。

【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
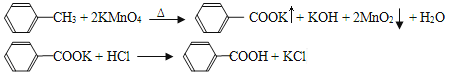
己知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。
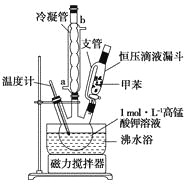
(1)图中冷凝管的进水口为________(填“a”或“b”)。支管的作用是___________。
(2)在本实验中,三领烧瓶最合适的容积___________(填字母)。
A.50mL | B.I00mL | C.200mL | D.250mL |
相对于用酒精灯直接加热,用沸水浴加热的优点是___________________。
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯
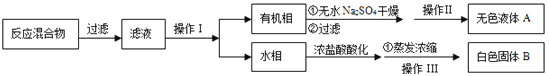
(3)操作Ⅰ的名称是 ;含有杂志的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是 。
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体加入水中,加热溶解,______。 | 得到白色晶体和无色溶液 | |
② | 取少重滤液于试管中,________。 | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________。 | _____________________ | 白色晶体是苯甲酸 |
纯度测定:称取1.220g产品,配成100ml甲醇溶液,取25.00ml溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
第一次 | 第二次 | 第三次 | 第四 | |
体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______________(填“偏大”、“偏小”或“不变”)。计算样品中苯甲酸纯度为______________。