题目内容
【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
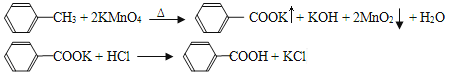
己知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。
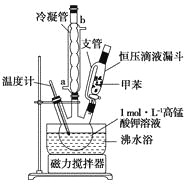
(1)图中冷凝管的进水口为________(填“a”或“b”)。支管的作用是___________。
(2)在本实验中,三领烧瓶最合适的容积___________(填字母)。
A.50mL | B.I00mL | C.200mL | D.250mL |
相对于用酒精灯直接加热,用沸水浴加热的优点是___________________。
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯
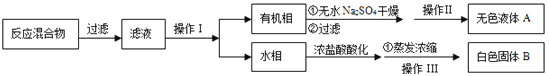
(3)操作Ⅰ的名称是 ;含有杂志的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是 。
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体加入水中,加热溶解,______。 | 得到白色晶体和无色溶液 | |
② | 取少重滤液于试管中,________。 | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________。 | _____________________ | 白色晶体是苯甲酸 |
纯度测定:称取1.220g产品,配成100ml甲醇溶液,取25.00ml溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
第一次 | 第二次 | 第三次 | 第四 | |
体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______________(填“偏大”、“偏小”或“不变”)。计算样品中苯甲酸纯度为______________。
【答案】(1)a (1分) 平衡压强,使甲苯顺利滴入三颈烧瓶 (1分)
(2)B (1分) 便于控制温度和使容器受热均匀 (2分) (3)分液,蒸馏 (2分)
(4)①冷却结晶,过滤 (2分) ②滴入稀HNO3和AgNO3溶液(1分)
③加热使其熔化,并测其熔点(1分) 白色晶体在122.4℃左右完全融化(1分)
(5)偏小(1分) 96%(2分)
【解析】试题分析:(1)根据逆流的冷却的效率高的原理可知,进水口应在冷凝管的下方a处,支管连接了恒压滴液漏斗中的液体上、下方,使恒压滴液漏斗中的液体上、下方的压强相等,便于甲苯顺利滴入三颈烧瓶;
(2)本实验中用到的液体体积约为55mL,所以选择100mL的三颈烧瓶,故选B,沸水浴加热便于控制温度和使容器受热均匀;
(3)一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按流程分离出苯甲酸和回收未反应的甲苯;所以操作Ⅰ是分离出有机相甲苯,用分液方法得到;操作Ⅱ是蒸馏的方法控制甲苯沸点得到纯净的甲苯液体;
(4)通过测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,推测白色固体B是苯甲酸与KCl的混合物,氯化钾可以用硝酸酸化的硝酸银溶液检验氯离子的存在;利用苯甲酸的溶解度特征在25℃和95℃时溶解度分别为0.3g和6.9g;利用不同温度下的溶解度,分离混合物,得到晶体后通过测定熔点判断是否为苯甲酸,所以实验方案及现象为:
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体B加入水中,加热,溶解,冷却结晶、过滤 | 得到白色晶体和无色溶液 | |
② | 取少量滤液于试管中,滴入适量的硝酸酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含有Cl- |
③ | 干燥白色晶体,加热使其熔化,测其熔点; | 白色晶体在122.4℃左右时完全熔化 | 白色晶体是苯甲酸 |
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则读取的溶液的体积小于实际用掉的溶液的体积,所以测定结果偏小;苯甲酸纯度=苯甲酸的质量/样品的质量×100%=(2.4×103mol×4×122g/mol)/1.22g×100%=96%。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】
(1)“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

①实验室在配制稀硫酸溶液时,下列操作可造成配制结果偏高的是________________。
A.采用仰视的方式量取浓硫酸 |
B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
C.定容时,俯视容量瓶刻度线 |
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度 |
②“服用维生素C,可防止二价亚铁离子被氧化”,由此可见维生素C具有_________性。
③加入KSCN溶液后,在未加新制氯水前,溶液中也产生红色,其可能的原因是 。
④加入氯水后发生的反应的离子方程式为 、 。
⑤在实验中发现放置一段时间,溶液的颜色会逐渐褪去。请你对溶液褪色的原因作出3种猜想。
编号 | 猜 想 |
甲 | |
乙 | |
丙 |
(2)正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含 mg FeSO4·7H2O 为片剂。