题目内容
10.高铁酸钠是一种高效多功能水处理剂.工业上常采用NaClO氧化法生产,反应原理为:在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品.反应方程式为:3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4↓+3NaCl+6NaNO3+5H2O(1)上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是Na2FeO4 在水溶液中易水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失.
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应方程式3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH.
(3)生产高铁酸钠的原料之一Fe(NO3)3用黑色粉末Fe(含有Fe3O4)与稀硝酸反应制备.准确称取该黑色粉末13.12g,加入200mL 4mol•L-1 HNO3搅拌,固体完全溶解,共收集到标准状况下2688mL的气体,经分析其中只含有NO,并测得此时溶液中c(H+)=0.4mol•L-1(设反应前后溶液体积不变).通过以上数据,计算该黑色粉末中Fe的质量分数.(写出计算过程,结果保留两位小数)
分析 (1)根据Na2FeO4在水溶液中阴离子水解平衡移动的影响因素结合实际应用来判断;
(2)根据反应信息知道:反应物是金属锌、高铁酸钠、产物是氢氧化铁、氢氧化锌来书写方程式;
(3)根据元素守恒和电荷守恒结合反应的过程来计算回答.
解答 解:(1)Na2FeO4在水溶液中会发生水解,并且水解后溶液呈碱性,如果在氢氧化钠溶液中,NaOH溶液呈碱性,会抑制其水解,有利于减少产品损失,
故答案为:Na2FeO4 在水溶液中水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失;
(2)根据反应信息知道:反应物是金属锌、高铁酸钠、产物是氢氧化铁、氢氧化锌,配平后的方程式为3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH,
故答案为:3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH;
(3)n(NO)=$\frac{2.688L}{22.4L/mol}$=0.12mol,溶液中还有H+,说明硝酸未反应完,所以溶液中只含Fe3+,溶液中有n(NO3-)=200mL×4mol•L-1/1000mL•L-1-0.12mol=0.68mol,根据电荷守恒 n(NO3-)×1=n(H+)×1+n(Fe3+)×3,n(Fe3+)=0.2mol,样品中所有铁元素物质的量为0.2mol.
设样品中Fe的物质的量为x,Fe3O4的物质的量为y
56g•mol-1×x+232g•mol-1×y=13.12g
x+3y=0.2mol,
解得:x=0.11mol,y=0.03mol
单质铁的质量分数为$\frac{0.11mol×56g/mol}{13.12g}$=0.47,
答:质量分数为0.47.
点评 本题综合考查学生盐的水解原理以及应用、原电池的工作原理以及元素以及化合物性质的计算等知识,属于综合知识的考查,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 化学键是一种作用力 | |
| B. | 化学键可以使离子间相互结合,也可以使原子间相互结合 | |
| C. | 化学反应过程中反应物化学键断裂,生成物化学键形成 | |
| D. | 氯化钠固体溶于水没有新物质生产,故没有破坏化学键 |
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 利用生物方法脱除生活污水中的氮和磷,防止水体富营养化 | |
| C. | PM 2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | 高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
| A. | 1:2:1混合的PbO2、Pb3O4、PbO | B. | 1:3:2混合的PbO2、Pb3O4、PbO | ||
| C. | 1:1:1混合的PbO2、Pb3O4、PbO | D. | 2:1:1混合的PbO2、Pb3O4、PbO |
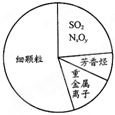 如图为雾霾的主要成分示意图.下列说法不正确的是( )
如图为雾霾的主要成分示意图.下列说法不正确的是( )| A. | 重金属离子可导致蛋白质变性 | |
| B. | 苯是最简单的芳香烃 | |
| C. | 向空气中大量排放SO2和NxOy都能引起酸雨和光化学烟雾 | |
| D. | 汽车尾气的大量排放是造成雾霾天气的人为因素之一 |
 通过 NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法正确的是( )
通过 NOx传感器可监测NOx的含量,其工作原理示意图如下,下列说法正确的是( )| A. | Pt 电极上发生的是氧化反应 | |
| B. | O2-向正极迁移 | |
| C. | 负极的电极反应式为:NO-2e-+O2-=NO2 | |
| D. | 正极的电极反应式为:O2+2H2O+4e-=4OH- |