题目内容
6.Ⅰ:(1)某温度(t℃)时,测得0.01mol•L-1 NaOH溶液的pH=13,此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va:Vb=10:1.(2)25℃时,pH=a的20mL的H2SO4溶液与c(H+)=10-b的200mL的NaOH溶液混合后(忽略体积变化),溶液呈中性,则a和b满足的关系a+b=15.
Ⅱ:常温下,取0.2mol•L-1 HCl溶液与0.2mol•L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)混合溶液中由水电离出的c (H+)>0.2mol•L-1HCl溶液中由水电离出的c (H+) (填“>、<或=”).
(2)求出混合物中下列算式的精确计算结果(填具体数字):
c (Cl-)-c (M+)=9.9×10-7mol•L-1,c (H+)-c (MOH)=1.0×10-8mol•L-1.
(3)若常温下取0.2mol•L-1 MOH溶液与0.1mol•L-1 HCl溶液等体积混合,测得混合溶液的pH<7,说明MOH的电离程度<(填“>、<或=”)MCl的水解程度.溶液中各离子浓度由大到小的顺序为c(Cl-)>c(M+)>c(H+)>c(OH-).
分析 Ⅰ、(1)c(H+)×c(OH-)=Kw,混合溶液呈中性,且硫酸和氢氧化钠都是强电解质,所以酸中氢离子物质的量和碱中氢氧根离子的物质的量相等;
(2)混合溶液呈中性,且硫酸和氢氧化钠都是强电解质,所以酸中氢离子物质的量和碱中氢氧根离子的物质的量相等,据此计算;
Ⅱ、(1)室温下取0.2mol•L-1HCl溶液与0.2mol•L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,说明得到的盐是强酸弱碱盐,其溶液呈酸性,含有弱根离子的盐促进水电离;
(2)根据物料守恒和电荷守恒计算离子浓度大小;
(3)室温下如果取0.2mol•L-1 MOH溶液与0.1mol•L-1 HCl溶液等体积混合,溶液中的溶质是MCl和MOH,测得混合溶液的pH<7,说明碱的电离程度小于盐的水解程度,根据电荷守恒判断离子浓度大小.
解答 解:Ⅰ、(1)混合溶液呈中性,且硫酸和氢氧化钠都是强电解质,所以酸中氢离子物质的量和碱中氢氧根离子的物质的量相等,pH=a的NaOH溶液中氢氧根离子浓度=10 a-15 mol/L,pH=b的H2SO4溶液氢离子浓度=10-b mol/L,10 a-15 mol/L×VaL=10-b mol/L×VbL且a=12,b=2,Z则Va:Vb=10:1,
故答案为:10:1;
(2)混合溶液呈中性,且硫酸和氢氧化钠都是强电解质,所以酸中氢离子物质的量和碱中氢氧根离子的物质的量相等,所以10-a×0.02L=$\frac{1{0}^{-14}}{1{0}^{-b}}$×0.2L,1-a=b-14,解得a+b=15,故答案为:a+b=15;
Ⅱ、(1)等体积等浓度的盐酸和MOH恰好反应生成盐,得到的盐溶液呈酸性,说明该盐是强酸弱碱盐,含有弱根离子的盐促进水电离,酸抑制水电离,所以混合溶液中水电离出的c(H+)>0.2 mol•L-1 HCl溶液中水电离出的c(H+),
故答案为:>;
(2)根据电荷守恒得c(Cl-)-c(M+)=c(H+)-c(OH-)=10-6 mol/L-10-8 mol/L=9.9×10-7mol•L-1,根据质子守恒得 c(H+)-c(MOH)=c(OH-)=1.0×10-8mol•L-1,
故答案为:9.9×10-7;1.0×10-8;
(3)室温下如果取0.2mol•L-1 MOH溶液与0.1mol•L-1 HCl溶液等体积混合,溶液中的溶质是MCl和MOH,测得混合溶液的pH<7,说明碱的电离程度小于盐的水解程度,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒知c(Cl-)>c(M+),盐中阴阳离子浓度大于氢离子和氢氧根离子浓度,所以溶液中各离子浓度由大到小的顺序为c(Cl-)>c(M+)>c(H+)>c(OH-),
故答案为:<;c(Cl-)>c(M+)>c(H+)>c(OH-).
点评 本题考查酸碱混合的定性判断和计算,为高频考点,侧重于学生的分析能力和计算能力的考查,根据电荷守恒和质子守恒分析弱电解质的电离及盐类水解,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 金属氧化物一定是碱性氧化物 | |
| B. | 胶体和其他分散系的本质区别是分散质粒子大小不同 | |
| C. | 生石灰、醋酸、纯碱、氯化钠对应的物质类别是氧化物、酸、碱、盐 | |
| D. | 酸性氧化物一定是非金属氧化物 |
| A. | 先后滴加紫色石蕊试液、BaCl2溶液,可以将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 | |
| B. | 用加入过量CuCl2溶液,再过滤,除去Cu(NO3)2溶液中混有的AgNO3 | |
| C. | 向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42- | |
| D. | 某固体在加入稀盐酸产生了无色无味且能使澄清石灰水变浑浊的气体,证明该固体一定含有CO32- |
①聚乙烯和乙烯
②甲醛和葡萄糖
③淀粉和纤维素
④蔗糖和麦芽糖
⑤聚乙烯和聚氯乙烯.
| A. | ①②⑤ | B. | ②③④ | C. | ①③⑤ | D. | ①②③ |
(1)在标准状况下,将a L由SO2和Cl2组成的混合气体通入200mL 0.1mol/L的Fe2(SO4)3溶液中,充分反应后,溶液的棕黄色变浅.向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3g.则混合气体中SO2的体积为0.896L,a的取值范围为:1.344<a<1.792.
(2)某温度下,SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ•mol-1.开始时在100L的密闭容器中加入4.0
mol SO2(g)和10.0mol O2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=3.33.
(3)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2,发生下列反应:
2SO2(g)+O2(g)?2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是ACF(填字母).
A.保持温度和容器体积不变,充入2mol SO3
B.保持温度和容器体积不变,充入2mol N2
C.保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2
D.保持温度和容器内压强不变,充入1mol SO3
E.升高温度
F.移动活塞压缩气体
(4)常温时,BaSO4的Ksp=1.08×10-10.现将等体积的BaCl2溶液与2.0×10-3mol/L的Na2SO4溶液混合.若要生成BaSO4沉淀,BaCl2溶液的最小浓度为2.16×10-7mol/L.
(5)N2O5是一种新型硝化剂,其性质和制备受到人们的关注.①一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.
如表为反应在T1温度下的部分实验数据:
| t/s | 0 | 50 | 100 |
| c(N2O5)/mol•L-1 | 5.0 | 3.5 | 2.4 |
②现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图所示,其中Y为CO2.
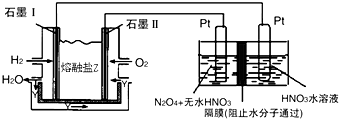
写出石墨I电极上发生反应的电极反应式H2+CO32--2e-=CO2+H2O.
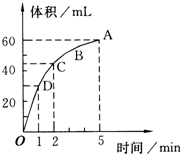 加入0.2mol的MnO2粉末于100mL过氧化氢的溶液中(密度为1.1g/mL),在标准状况下放出气体的体积和时间的关系如图所示,回答下列问题:
加入0.2mol的MnO2粉末于100mL过氧化氢的溶液中(密度为1.1g/mL),在标准状况下放出气体的体积和时间的关系如图所示,回答下列问题: