题目内容
在硫酸的工业生产中,通过下列反应使SO2转化为SO3:2SO2+O2(1)在生产中常用过量的空气是为了___________________。
(2)加热到400—500 ℃是由于___________。
(3)压强应采用__________ (填“高压”或“常压”)。原因是____________________________。
(4)常用浓H2SO4来吸收SO3,而不是用水,是因为____________________。
(5)尾气中的SO2必须回收,是因为____________________。
(1)增大氧气的浓度,使平衡向正反应方向移动,提高了二氧化硫的转化率,使成本高的二氧化硫得到充分利用
(2)400—500 ℃是催化剂的活性温度,选择此温度可提高反应速率,缩短到达平衡所需的时间
(3)常压 因为常压下SO3体积分数已达91%,若再加压对设备及动力系统要求高、成本高,生产效益反而会降低
(4)用水吸收SO3会形成酸雾,使吸收的速率减慢
(5)SO2有毒,避免对环境的污染

练习册系列答案
相关题目
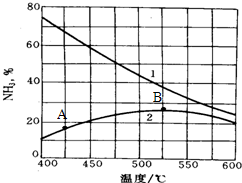
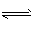 2SO3(g) △H <0。已知常压下SO3体积分数为91%,试回答:
2SO3(g) △H <0。已知常压下SO3体积分数为91%,试回答: