题目内容
(Ⅰ)多项选择题下列关于化工生产的叙述正确的是
A.炼钢就是在高炉中用还原剂把铁从铁矿石中还原出来
B.离子交换膜法制碱工业中,氢氧化钠在电解槽的阴极区产生
C.工业制硫酸中,三氧化硫是在吸收塔内用98%的硫酸吸收
D.黏土是生产陶瓷、玻璃和水泥的共同原料
(Ⅱ)氨是重要的无机化工产品之一,在国民经济中占有重要地位.世界上的氨除少量从焦炉气中回收副产外,绝大部分是合成的氨.海南岛的南海北部湾莺歌海海域有着丰富的天然气气田,利用此资源在东方市八所港建有一家大型的合成氨化肥厂.
(1)写出该化肥厂生产H2的化学反应方程式
(2)在硫酸的工业生产中,往往会增大O2的比例来提高SO2的转化率,在合成氨生产中是否会采用相同的方法,请说明理由.
(3)在制取原料气体的过程中,常混有一些杂质,在进入合成塔之前必须将杂质除去,原因是
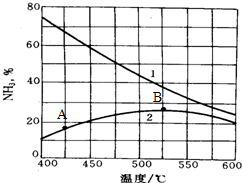
(4)下图是氨的产率与温度的关系,曲线1表示平衡时氨的产率,曲线2表示反应进行一段时间但还未达到平衡时氨的含量.请分析A点氨的含量小于B的原因
(5)在合成氨的生产过程中会产生大量CO2,该化肥厂与俄罗斯塔氏集团合作,利用这些CO2建设一个年产52万吨的小颗粒尿素加工厂,再进一步加工成氮磷钾复合肥,请写出该合成尿素反应的化学方程式
分析:(Ⅰ)A、根据炼钢主要是用氧化剂把生铁里过多的碳和其它杂质氧化而除去进行分析;
B、根据电解原理判断离子交换膜法制碱工业中氢氧化钠的出处;
C、用水吸收三氧化硫,反应放出的热量易导致酸雾形成,应该使用浓硫酸稀释;
D、根据陶瓷、水泥和玻璃的原料进行判断;
(Ⅱ)(1)化肥厂利用甲烷与水反应生成二氧化碳和氢气,据此写出反应的化学方程式;
(2)根据合成氨的反应中,氮气和氢气的转化率较低进行分析;
(3)在制取原料气体中含有的杂质会造成催化剂中毒,较低了催化剂的催化效果;可以用碳酸钾溶液吸收氮气和氢气中的二氧化碳;
(4)根据A、B两点温度不同分析A点氨的含量小于B的原因;根据在500℃时催化剂的反应活性最大分析;
(5)根据反应物为二氧化碳和氨气,生成产物为尿素写出反应的化学方程式;从环境污染和经济效益方面分析该设计的优点.
B、根据电解原理判断离子交换膜法制碱工业中氢氧化钠的出处;
C、用水吸收三氧化硫,反应放出的热量易导致酸雾形成,应该使用浓硫酸稀释;
D、根据陶瓷、水泥和玻璃的原料进行判断;
(Ⅱ)(1)化肥厂利用甲烷与水反应生成二氧化碳和氢气,据此写出反应的化学方程式;
(2)根据合成氨的反应中,氮气和氢气的转化率较低进行分析;
(3)在制取原料气体中含有的杂质会造成催化剂中毒,较低了催化剂的催化效果;可以用碳酸钾溶液吸收氮气和氢气中的二氧化碳;
(4)根据A、B两点温度不同分析A点氨的含量小于B的原因;根据在500℃时催化剂的反应活性最大分析;
(5)根据反应物为二氧化碳和氨气,生成产物为尿素写出反应的化学方程式;从环境污染和经济效益方面分析该设计的优点.
解答:解:(Ⅰ)A、炼铁主要是用还原剂把铁从铁矿石里还原出来,而炼钢主要是用氧化剂把生铁里过多的碳和其它杂质氧化而除去,故A错误;
B、电解槽中阴极发生还原反应生成氢气,同时溶液中生成了氢氧根离子,与钠离子结合生成氢氧化钠,故B正确;
C、吸收塔中SO3如果用水吸收,发生反应:SO3+H2O═H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,最终得到“发烟”硫酸,故C正确;
D、粘土是生成陶瓷、水泥的主要原料,而生产玻璃的原料是纯碱、石灰石和石英,没有用到粘土,故D错误;
故选BC;
(Ⅱ)(1)用天然气在高温、催化剂作用下与水蒸气反应来制备氢气和二氧化碳,反应的化学方程式为:CH4+4H2O
CO2+4H2,
故答案为:CH4+4H2O
CO2+4H2;
(2)合成氨工业中氮气、氢气的转化率很低,需要不断的循环利用,故不需要提高某一种反应物的量,否则会造成资源浪费,
故答案为:不用;因为合成氨工业中氮气、氢气的转化率很低,需要不断的循环利用,故不需要提高某一种反应物的量,否则会造成资源浪费;
(3)在制取原料气体的过程中,常混有一些杂质,杂质会造成催化剂中毒,使催化剂失去活性,在进入合成塔之前必须将杂质除去;将一氧化碳氧化成二氧化碳,然后可以利用碳酸钾溶液吸收二氧化碳,
故答案为:杂质会造成催化剂中毒,使催化剂失去活性;碳酸钾溶液;
(4)由于B点的反应温度高于A点,故反应速率快,单位时间内生成氨气的量多,所以A点氨的含量小于B;在400℃时,虽然氨气的产率较高,但是反应速率较慢,并且在500℃时催化剂的反应活性最大,故工业生产选择500℃而不用400℃,
故答案为:B点的反应温度高于A点,故反应速率快,单位时间内生成氨气的量多;400℃时,虽然氨气的产率较高,但是反应速率较慢,并且在500℃时催化剂的反应活性最大,故工业生产选择500℃;
(5)氨气与二氧化碳反应生成尿素,合成尿素反应的化学方程式为:CO2+2NH3
CO(NH2)2+H2O;该设计的优点为:利用生成氢气时产生的废气来生成新产品,一方面减少二氧化碳的排放,减小对环境的污染;另一方面开放新产品,提高生成的附加值,提高经济效益,
故答案为:CO2+2NH3
CO(NH2)2+H2O;利用生成氢气时产生的废气来生成新产品,一方面减少二氧化碳的排放,减小对环境的污染;另一方面开放新产品,提高生成的附加值,提高经济效益.
B、电解槽中阴极发生还原反应生成氢气,同时溶液中生成了氢氧根离子,与钠离子结合生成氢氧化钠,故B正确;
C、吸收塔中SO3如果用水吸收,发生反应:SO3+H2O═H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,最终得到“发烟”硫酸,故C正确;
D、粘土是生成陶瓷、水泥的主要原料,而生产玻璃的原料是纯碱、石灰石和石英,没有用到粘土,故D错误;
故选BC;
(Ⅱ)(1)用天然气在高温、催化剂作用下与水蒸气反应来制备氢气和二氧化碳,反应的化学方程式为:CH4+4H2O
| ||
| 催化剂 |
故答案为:CH4+4H2O
| ||
| 催化剂 |
(2)合成氨工业中氮气、氢气的转化率很低,需要不断的循环利用,故不需要提高某一种反应物的量,否则会造成资源浪费,
故答案为:不用;因为合成氨工业中氮气、氢气的转化率很低,需要不断的循环利用,故不需要提高某一种反应物的量,否则会造成资源浪费;
(3)在制取原料气体的过程中,常混有一些杂质,杂质会造成催化剂中毒,使催化剂失去活性,在进入合成塔之前必须将杂质除去;将一氧化碳氧化成二氧化碳,然后可以利用碳酸钾溶液吸收二氧化碳,
故答案为:杂质会造成催化剂中毒,使催化剂失去活性;碳酸钾溶液;
(4)由于B点的反应温度高于A点,故反应速率快,单位时间内生成氨气的量多,所以A点氨的含量小于B;在400℃时,虽然氨气的产率较高,但是反应速率较慢,并且在500℃时催化剂的反应活性最大,故工业生产选择500℃而不用400℃,
故答案为:B点的反应温度高于A点,故反应速率快,单位时间内生成氨气的量多;400℃时,虽然氨气的产率较高,但是反应速率较慢,并且在500℃时催化剂的反应活性最大,故工业生产选择500℃;
(5)氨气与二氧化碳反应生成尿素,合成尿素反应的化学方程式为:CO2+2NH3
| ||
故答案为:CO2+2NH3
| ||
点评:本题考查了合成氨、产物的百分含量随浓度、时间的变化曲线,本题难度稍大,涉及了化学方程式的书写、实验方案的评价及温度、压强对化学反应速率和化学平衡的影响等知识,试题综合性强,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力.

练习册系列答案
相关题目