题目内容
【题目】硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O],其相对分子质量为392,在空气中不易被氧化,易溶于水,不溶于乙醇,100℃时易失去结晶水。现用FeSO4溶液与(NH4)2SO4反应,制取硫酸亚铁铵晶体,其流程如图所示:

(1)“混合反应”时温度需控制在70~80℃,可采取的措施是___________,该过程中乙醇的作用是___________。
(2)现对制得的硫酸亚铁铵晶体进行纯度测定:准确称取4.000g上述硫酸亚铁铵晶体置于锥形瓶中溶解,加适量稀硫酸酸化,用0.100mol·L-1标准KMnO4溶液进行反应,当![]() 恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00mL。
恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00mL。
已知:![]() +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
①若用稀盐酸替代稀硫酸进行酸化,则实际消耗的标准KMnO4溶液的体积___________20.00mL。(填“大于”或“小于”或“等于”)
②试通过计算,求该硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]的纯度(写出计算过程)___________
【答案】水浴加热 降低硫酸亚铁铵晶体溶解度,利于析出。 大于 98%
【解析】
FeSO4和(NH4)2SO4混合,得到(NH4)2Fe(SO4)2的水溶液,根据信息,硫酸亚铁铵不溶于乙醇,加入乙醇,降低(NH4)2Fe(SO4)2·6H2O的溶解度,使之析出,过滤得到晶体,经洗涤、干燥得到产品。
(1)混合反应时需要控制温度在70-80℃,可采取水浴加热,可以控制加热温度,且受热更加均匀;根据信息,(NH4)2Fe(SO4)2·6H2O不溶于乙醇,加入乙醇,可以降低(NH4)2Fe(SO4)2·6H2O的溶解度,使之析出;
(2)①KMnO4能够氧化Cl-,若用盐酸酸化高锰酸钾,消耗的高锰酸钾的量会增加,则实际消耗的标准KMnO4溶液的体积大于20.00mL;
②消耗KMnO4的量n(KMnO4)=0.1mol·L-1×20.00mL×10-3mL·L-1=0.002mol·L-1,根据化学方程式,则n(Fe2+)=5n(KMnO4)=5×0.002mol·L-1=0.01mol,根据Fe守恒,n[(NH4)2Fe(SO4)2·6H2O]=n(Fe2+)=0.01mol,m[(NH4)2Fe(SO4)2·6H2O]=0.01mol×392g·mol-1=3.92g,则纯度为![]() 。
。

【题目】某学生为探究AgCl沉淀的溶解和转化,其实验方案及记录如下:
步骤和现象 | 现象 |
Ⅰ.将等体积等浓度的AgNO3溶液和NaCl溶液混合,过滤,得滤液X和白色沉淀Y | |
Ⅱ.向滤液X 中滴加几滴饱和KI溶液 | 生成黄色沉淀M |
Ⅲ.取少量白色沉淀Y,滴加几滴饱和Na2S溶液 | 沉淀Y 转化为黑色沉淀Z |
Ⅳ.取少量白色沉淀Y,滴加几滴浓氨水 | 沉淀Y逐渐溶解 |
(1)由步骤Ⅱ的现象可推测,滤液 X 中除了含有Na+、NO3-,还含有的离子有_____。
(2)写出步骤Ⅲ中生成黑色沉淀 Z 的离子方程式为_________________,白色沉淀Y 转化为黑色沉淀 Z 的主要原因是___________。
(3)已知:Ag+ + 2NH3· H2OAg(NH3)2++2H2O,用平衡移动原理解释步骤Ⅳ中加入浓氨水沉淀逐渐溶解的原因__________________。
(4)为了进一步探究银的难溶化合物沉淀溶解的多样性,该同学又做了如下对比实验 V:
①取少量黑色沉淀 Z 和黄色沉淀 M,分置于两支试管中
②然后分别滴加同体积同浓度的稀硝酸,观察到黄色沉淀 M 不溶解,黑色沉淀 Z 溶解,并且有无色气体产生。综合实验Ⅱ至实验 V 的信息,下列预测正确的是__________
A.黑色沉淀 Z 比黄色沉淀 M 更难溶于水
B.黑色沉淀 Z 溶解于稀硝酸是因为发生了氧化还原反应
C.由步骤Ⅳ可以推测:实验室可用氨水洗涤银镜反应后的试管
D.在步骤Ⅳ之后,继续滴加浓硝酸后又有 AgCl 沉淀生成
【题目】纳米TiO2具有十分宝贵的光学性质,在汽车工业及诸多领域都显示出美好的发展前景。如图是以硫酸氧钛为原料制备纳米二氧化钛的工艺流程图:
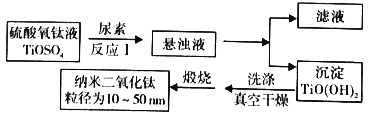
回答下列问题:
(1)反应1中发生两个反应,其一是尿素[CO(NH2)2]与H2O反应生成CO2和NH3·H2O,则另一反应的离子方程式为__。
(2)判断TiO(OH)2沉淀是否洗净的实验操作和现象是:__。
(3)为了减少制备过程中的“三废”排放,将上述流程中的“滤液”经过__、__、__(填基本操作)即可回收__(填化学式)。
(4)为研究反应温度、反应时间、反应物物质的量配比等因素对制备纳米二氧化钛产率的影响,设计如下实验。
实验编号 | 反应温度/℃ | 反应时间/h | 反应物物质的量配比n[CO(NH2)2]:n[TiO(OH)2] |
① | 90 | 1 | 2:1 |
② | 90 | 2 | 3:1 |
③ | 90 | 1 | |
④ | 110 | 2 | 3:1 |
实验②和④的实验目的是__,实验③中反应物物质的量配比为__。
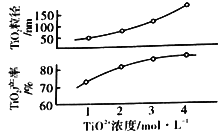
(5)反应Ⅰ中TiO2+浓度对TiO2的产率和粒径的影响如图。结合图中信息,你认为为达到工艺目的,最合适的TiO2+浓度为__。