题目内容
16.工业上以CaO和HNO3为原料制备Ca(NO3)2•6H2O晶体.为确保制备过程中既不补充水分,也无多余的水分,所用硝酸溶液中溶质的质量分数应为( )| A. | 53.8% | B. | 58.3% | C. | 60.3% | D. | 70.0% |
分析 工业上以CaO和HNO3为原料制备Ca(NO3)2•6H2O晶体.为确保制备过程中既不补充水分,也无多余的水分,也就是硝酸溶液中的水全部参与化学反应生成Ca(NO3)2•6H2O晶体,反应方程式为CaO+2HNO3+5H2O═Ca(NO3)2•6H2O,设硝酸的质量为126g,根据方程式可知硝酸溶液中水的质量为90g,据此结合质量分数的定义计算硝酸溶液中溶质的质量分数.
解答 解:工业上以CaO和HNO3为原料制备Ca(NO3)2•6H2O晶体.为确保制备过程中既不补充水分,也无多余的水分,也就是硝酸溶液中的水全部参与化学反应生成Ca(NO3)2•6H2O晶体,反应方程式为:CaO+2HNO3+5H2O═Ca(NO3)2•6H2O,设硝酸的质量为126g,则:
CaO+2HNO3+5H2O═Ca(NO3)2•6H2O
126g 90g
因此硝酸溶液中溶质的质量分数为$\frac{126g}{126g+90g}$×100%=58.3%,
故选B.
点评 本题考查根据化学方程式计算溶液中溶质的质量分数,题目难度中等,正确书写反应的方程式为解答关键,试题旨在培养学生的理解能力和计算能力.

练习册系列答案
相关题目
6.下列说法正确的是( )
| A. | 按系统命名法,有机物 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 | |
| B. | 苯、甲苯、二甲苯互为同系物,均能使酸性高锰酸钾溶液褪色 | |
| C. | 等质量的苯、乙炔、乙烯和甲烷分别在氧气中充分燃烧,所消耗的氧气的量依次增加 | |
| D. | 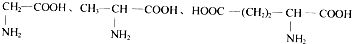 三种氨基酸之间脱水,最多可生成6种二肽 三种氨基酸之间脱水,最多可生成6种二肽 |
11.美国《Science》杂志曾经报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰.有关原子晶体干冰的推断错误的是( )
| A. | 有很高的熔点和沸点 | B. | 易汽化,可用作制冷材料 | ||
| C. | 含有极性共价键 | D. | 硬度大,可用作耐磨材料 |
1.化学中常用图象直观地描述化学反应的进程或结果.只改变一个条件,则下列对图象的解读正确的是( )
| A. | 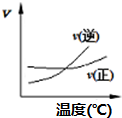 A2(g)+3B2(g)?2AB3(g)如图说明此反应的正反应是吸热反应 | |
| B. | 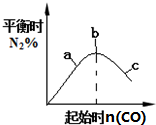 4CO(g)+2NO2(g)?N2(g)+4CO2(g)如图说明NO2的转化率b>a>c | |
| C. |  N2(g)+3H2(g)?2NH3(g)如图说明t秒时合成氨反应达到平衡 | |
| D. |  2A(g)+2B(g)?3C(g)+D(?)如图说明生成物D一定是气体 |
8.在含有0.6molCl-、0.8molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.则( )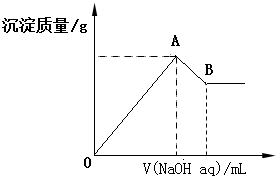

| A. | x=$\frac{2a}{5-a}$ | |
| B. | x的取值范围是0<x<$\frac{11}{32}$ | |
| C. | A点横坐标的值随x发生变化 | |
| D. | 若B点横坐标为200mL时,c(NaOH)=7.0mol/L |
5.下列说法正确的是( )
| A. | 按系统命名法,有机物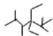 的名称是 2,2,4,5-四甲基-3,3-二乙基己烷 的名称是 2,2,4,5-四甲基-3,3-二乙基己烷 | |
| B. | 苯、甲苯、二甲苯互为同系物,均能使酸性高锰酸钾溶液褪色 | |
| C. | 等质量的苯、乙炔(CH≡CH)、乙烯和甲烷分别在氧气中充分燃烧,所消耗的氧气的量依次增加 | |
| D. | 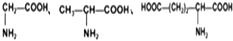 三种氨基酸之间脱水,最多可生成6种二肽 三种氨基酸之间脱水,最多可生成6种二肽 |
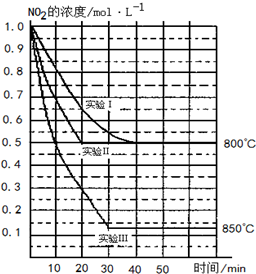 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol•L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol•L-1)随时间(min)的变化如图所示.请回答下列问题:
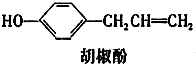 胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )
胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法,其中正确的是( )