题目内容
已知某粒子的质子数,则可确定的( )
| A、中子数 | B、最外层电子数 |
| C、核电荷数 | D、相对原子质量 |
考点:质子数、中子数、核外电子数及其相互联系,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:在任何粒子中,质子数=核电荷数,相对原子质量=质子数+中子数,利用上述知识可以做出正确判断.
解答:
解:A、根据题目条件,无法确定中子数,故A错误;
B、由于不知中子数,故无法确定电子数,所以无法知道最外层电子数,故B错误;
C、质子数=核电荷数,故可以确定质子数,故C正确;
D、由于不知中子数,故无法确定相对原子质量,故D错误.
故选C.
B、由于不知中子数,故无法确定电子数,所以无法知道最外层电子数,故B错误;
C、质子数=核电荷数,故可以确定质子数,故C正确;
D、由于不知中子数,故无法确定相对原子质量,故D错误.
故选C.
点评:本题难度不大,利用质子数电子数等于核电荷数的规律解决是解题的关键,属基础性知识考查.

练习册系列答案
相关题目
芳香族化合物A的分子式为C7H8O,它与Na反应有气体产生.满足条件的同分异构体的数目是( )
| A、4 | B、3 | C、2 | D、1 |
常温下把氨水滴到盐酸中,当c(NH4+)=c(Cl-)时,混合液的pH值( )
| A、等于7 | B、大于7 |
| C、小于7 | D、无法判断 |
已知:25℃、101kPa时,C(s)和CO(g)的燃烧热分别为393.5kJ/mol和283.0kJ/mol,Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H=+489.0kJ/mol.则4Fe(s)+3O2(g)═2Fe2O3(s)△H=( )
| A、+663.5kJ/mol |
| B、+3081kJ/mol |
| C、-1641.0kJ/mol |
| D、-2507.0kJ/mol |
下列说法正确的是( )
| A、钠的金属活泼性大于铜,在溶液中钠可以置换出铜 |
| B、使用托盘天平称量固体药品时左码右物,可能会导致所配溶液浓度偏低 |
| C、工业上电解熔融MgCl2制取镁,也可电解熔融AlCl3制取铝 |
| D、碳、钠与O2反应时,由于O2的量不同,可分别生成CO、CO2和Na2O、Na2O2 |
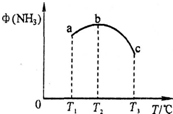 合成氨和制备硝酸是两种重要的化工生产,重庆某化工厂将合成氨与制备硝酸进行连续生产.
合成氨和制备硝酸是两种重要的化工生产,重庆某化工厂将合成氨与制备硝酸进行连续生产. 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题: