题目内容
下列叙述正确的是
| A.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
B.2SO2(g) + O2(g) 2SO3(g)的正、逆反应的平衡常数K随温度的变化可用上图表示 2SO3(g)的正、逆反应的平衡常数K随温度的变化可用上图表示 |
C.2NO+2CO 2CO2+N2的ΔH<0,常温下该反应一定能自发进行 2CO2+N2的ΔH<0,常温下该反应一定能自发进行 |
| D.25°C时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)减小 |
B
解析试题分析:A、不正确,pH=5的CH3COOH溶液抑制水电离,pH=5的NH4Cl溶液中NH4+ 水解,促进水电离,水的电离程度前者远小于后者;B、正确,正逆反应的平衡常数互为倒数,图正确;C、不正确,ΔH<0,△S<0,ΔH—T△S,温度较低时可能自发;D、不正确,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增加。选B。
考点:基本概念

练习册系列答案
相关题目
已知反应X (g)+Y (g)  n Z (g) △H > 0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是
n Z (g) △H > 0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是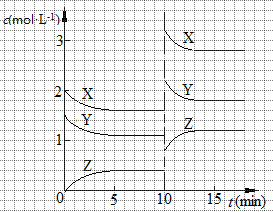
| A.反应方程式中n=1 |
| B.10 min时,曲线发生变化的原因是升高温度 |
| C.10 min时,曲线发生变化的原因是增大压强 |
| D.0~5 min内,用X表示的反应速率为v(X)="0.08" mol·L-1·min-1 |
已知4NH3+5O2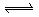 4NO+6H2O,若化学反应速率分别是用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)〔单位:mol/(L·s)〕表示,则正确的关系是
4NO+6H2O,若化学反应速率分别是用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)〔单位:mol/(L·s)〕表示,则正确的关系是
| A.4/5υ(NH3) = υ(O2) | B.5/6υ(O2) =υ(H2O) |
| C.2/3υ(NH3) = υ(H2O) | D.4/5υ(O2) = υ(NO) |
溴水中存在着如下的平衡:Br2+H2O HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是
HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是
| A.加压 | B.加入NaF晶体 | C.通入SO2气体 | D.加入NaI晶体 |
已知:2SO2(g)+O2(g) 2SO3(g) △H=—196.6kJ·mol—1,向密闭容器中加入2mol SO2(g)和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是
2SO3(g) △H=—196.6kJ·mol—1,向密闭容器中加入2mol SO2(g)和1mol O2,一定条件下反应达到平衡,在t2和t4时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如下图所示,下列说法正确的是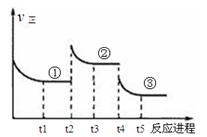
注:t1~t2、t3~t4、t5之后各时间段表示达到平衡状态①、②、③。
| A.t2~t3时间段,平衡向逆反应方向移动 |
| B.平衡状态①和②,平衡常数K值相同 |
| C.平衡状态①和②,SO2转化率相同 |
| D.t4时刻改变的条件是减小压强 |
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 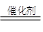 2CO2(g)+S(l) ΔH<0
2CO2(g)+S(l) ΔH<0
若反应在恒容的密闭容器中进行,下列有关说法正确的是
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
下列对化学反应方向的叙述,正确的是
| A.室温下不能自发进行的反应,在高温下有可能自发进行 |
| B.熵增加有利于反应的自发进行,熵减少的反应常温下都不会自发进行 |
| C.非自发反应在任何情况下都不会发生 |
| D.ΔH-TΔS作为化学反应方向的判据,在任何条件下都适用 |
T1℃时,向容积为2L的密闭容器中充入一定量的A气体和B气体,发生如下反应:
A(g)+2B (g)  C(g)
C(g)
反应过程中测定的部分数据见下表:
| 反应时间/min | n(A)/mol | n(B)/ mol |
| 0 | 1.00 | 1.20 |
| 10 | 0.50 | |
| 30 | | 0.20 |
下列说法正确的是
A.前10 min内反应的平均速率为v(C)=0.050 mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.50 mol A气体和0.60 mol B气体,到达平衡时,n(C)<0.25 mol
C.若密闭容器体积可变,其他条件不变,在达到平衡后持续缩小容器体积,则平衡一直会正向移动
D.温度为T2℃时(T1>T2),上述反应平衡常数为20,则正反应为放热反应
 2Q(g)+ nR(g)达到平衡时测得 X的转化率为25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是
2Q(g)+ nR(g)达到平衡时测得 X的转化率为25%,此时混合气体的体积为6.5L。则该反应方程式中的n值是