题目内容
【题目】某课外小组分别用下图所示装置对原电池和电解原理进行实验探究。

请回答:
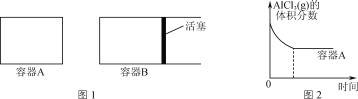
I.用图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是_________(填字母序号)。
A.铝 | B.石墨 | C.银 | D.铂 |
(2)N极发生反应的电极反应式为____________________。
(3)实验过程中,SO42-_________(填“从左向右”、“从右向左”或“不”)移动;
滤纸上能观察到的现象有___________________。
II.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH___________(填“增大” 、“减小”或“不变”)。电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O 和_______________。
(5)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
【答案】A 2H++ 2e-= H2↑(2H2O + 2e-= H2↑+ 2OH-) 从右向左 滤纸上有红褐色斑点产生 增大 4OH-- 4e-= 2H2O + O2↑ 0.28
【解析】
I(1)若用铝代替铜,铝的活泼性大于锌,铝作负极,石墨、银、铂代替铜,锌依然作负极,不改变原电极反应,答案选A;
(2)左面的装置为原电池,锌为负极,右面的装置为电解池,N极与负极连接,N为阴极,电解反应为2H++ 2e-= H2↑或(2H2O + 2e-= H2↑+ 2OH-);
(3)SO42-移向负极,所以从右向左移动;M极生成亚铁离子,与氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧化为红褐色的氢氧化铁,所以滤纸上有红褐色斑点产生;
II(4)X极为阴极,电极反应为2H2O + 2e-= H2↑+ 2OH-,X极区溶液的pH增大;两极均有气体产生,所以Y极发生的电极反应还有4OH-- 4e-= 2H2O + O2↑;
(5)X极收集到672 mL氢气,转移电子0.06mol;在Y极收集到168 mL氧气,转移电子0.03mol,根据电子守恒,发生Fe-6e-+8OH-=FeO42-+4H2O反应转移电子0.03mol,所以消耗铁0.005mol,质量减少0.005mol×56g/mol=0.28g。

【题目】现有A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素的核内质子数之和为56,在元素周期表中的位置如图所示,1 mol E的单质可与足量酸反应,能产生33.6L H2(在标准状况下);E的阳离子与A的阴离子核外电子层结构相同。
A | ||
B | C | D |
回答下列问题:
(1)写出元素A名称______,元素B符号________,E原子电子式________
(2)C的简单离子结构示意图为_____________
(3)B单质在A单质中燃烧,反应现象是___________,生成物的化学式为___________
(4)A与E形成的化合物的电子式为__________,它的性质决定了它在物质的分类中应属于____________(酸性氧化物/碱性氧化物/两性氧化物)
(5)向D与E形成的化合物的水溶液中滴入烧碱溶液至过量,此过程中观察到的现象是_________,写出化合物DE与过量烧碱反应的化学反应方程式________。