��Ŀ����
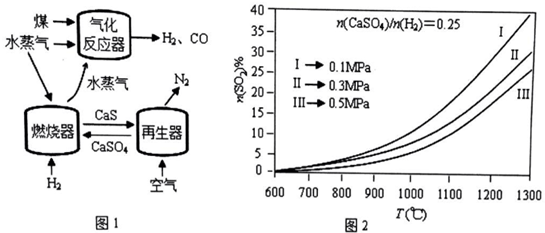
12����1�����飨SinH2n+2���ķе�������Է��������ı仯��ϵ��ͼ1��ʾ���������ֱ仯��ϵ��ԭ���ǹ������Է�������Խ���Ӽ䷶�»���Խ�е�Խ�ߣ�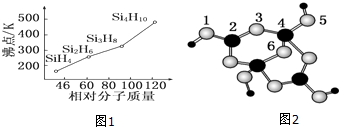
��2����ɰ�Ǻ��ᾧˮ���������ƣ���������Xm-����B��O��H����Ԫ�أ������ģ����ͼ2��ʾ��
��Xm-�У���ԭ�ӹ�����ӻ�������sp2��sp3����λ��������4��5����5��4��ԭ��֮�䣨��ԭ�ӵ����ֱ�ţ���m=2�������֣���
��3�����ɽ��������Ni��CO��n������ԭ�Ӽ۵������������ṩ��������֮��Ϊ18����n=4��CO��N2�ṹ���ƣ�CO�����ڦҼ���м�����֮��Ϊ1��2��
���� ��1�����Ӿ�����۷е�������Ӽ������������ȣ����Ӽ�����������Է������������ȣ�
��2������ͼ֪��Bԭ�Ӽ۲���ӶԸ�����3�IJ���sp2�ӻ�����4�IJ���sp3�ӻ������пչ����ԭ�Ӻͺ��йµ��ӶԵ�ԭ��֮�����γ���λ��������ΪH4B4O9m-��HԪ��Ϊ+1�ۡ�BԪ��Ϊ+3�ۡ�OԪ��Ϊ-2�ۣ��ݴ��ж�mֵ��
��3��Ni��28��Ԫ�أ���۵�������10��ÿ��CO�ṩ������Ϊ2�����ɽ��������Ni��CO��n������ԭ�Ӽ۵������������ṩ��������֮��Ϊ18����n=$\frac{18-10}{2}$��ÿ�����������к���1���Ҽ���2���м���CO��N2�ṹ���ƣ��ݴ˼���CO�����ЦҼ���м�����֮�ȣ�
��� �⣺��1�����Ӿ�����۷е�������Ӽ������������ȣ����Ӽ�����������Է������������ȣ�����������Է����������������۷е������ߣ��ʴ�Ϊ���������Է�������Խ���Ӽ䷶�»���Խ�е�Խ�ߣ�
��2������ͼ֪��Bԭ�Ӽ۲���ӶԸ�����3�IJ���sp2�ӻ�����4�IJ���sp3�ӻ���
���пչ����ԭ�Ӻͺ��йµ��ӶԵ�ԭ��֮�����γ���λ����Bԭ�Ӻ��пչ����Oԭ�Ӻ��йµ��Ӷԣ�4��5����5��4��ԭ��֮�������λ��������ΪH4B4O9m-��HԪ��Ϊ+1�ۡ�BԪ��Ϊ+3�ۡ�OԪ��Ϊ-2�ۣ�����m=2��
�ʴ�Ϊ��sp2��sp3��4��5����5��4����2��
��3��Ni��28��Ԫ�أ���۵�������10��ÿ��CO�ṩ������Ϊ2�����ɽ��������Ni��CO��n������ԭ�Ӽ۵������������ṩ��������֮��Ϊ18����n=$\frac{18-10}{2}$=4��ÿ�����������к���1���Ҽ���2���м���CO��N2�ṹ���ƣ�����CO�����ЦҼ���м�����֮��Ϊ1��2��
�ʴ�Ϊ��4��1��2��
���� ���⿼���ʽṹ�����ʣ��漰�����ɼ������ԭ���ӻ������ʽṹ�����Ӿ����۷е��֪ʶ�㣬Ϊ��Ƶ���㣬֪����λ���Ĺ������������ж�ԭ���ӻ���ʽ����Ŀ�ѶȲ���

| A�� | ������ʹ����Ӧ�����ʷ�����Ӧ | |
| B�� | �����ڻ�ѧ��Ӧǰ��ѧ���ʺ����������� | |
| C�� | �������ܸı仯ѧ��Ӧ���� | |
| D�� | �κλ�ѧ��Ӧ������Ҫ���� |
| A�� | C6H5CH2CH2OH��C6H5OH��Ϊͬϵ�� | |
| B�� | CH3CHO��CH3COOH��һ�������¾���������������ͭ��Ӧ | |
| C�� | 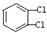 �� �� 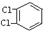 ��Ϊͬ���칹�� ��Ϊͬ���칹�� | |
| D�� | H2O��D2O��Ϊͬ�������� |
| A�� | ���³�ѹ�£�48g O3���е���ԭ����Ϊ3NA | |
| B�� | 17g��OH-�����к��еĵ�����Ϊ0.1NA | |
| C�� | ���³�ѹ�£�11.2L�����������е�ԭ����ΪNA | |
| D�� | 2.4g����þ��Ϊþ����ʱʧȥ�ĵ�����Ϊ0.1NA |
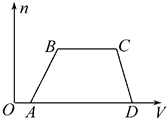
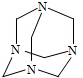 ������Ʒ�ںϳɡ�ҽҩ��Ⱦ�ϵȹ�ҵ���й㷺��;����ṹʽ��ͼ��ʾ������ȩˮ��Һ�백ˮ����������Ƶ�������Ʒ����ԭ����ȫ��Ӧ����������Ʒ�����ȩ�백�����ʵ���֮��Ϊ��������
������Ʒ�ںϳɡ�ҽҩ��Ⱦ�ϵȹ�ҵ���й㷺��;����ṹʽ��ͼ��ʾ������ȩˮ��Һ�백ˮ����������Ƶ�������Ʒ����ԭ����ȫ��Ӧ����������Ʒ�����ȩ�백�����ʵ���֮��Ϊ��������