题目内容
7.已知M、N两种金属都能与稀硫酸反应放出氢气,现有M、N两种金属片、稀硫酸、导线、烧杯,请你用原电池原理设计装置比较M、N 的金属性强弱.
(1)在右边方框2中画出装置图.
(2)若实验时,M上有气泡,N上没气泡,则M的最高价氧化物对应的水化物的碱性比N的最高价氧化物对应的水化物的碱性比弱(填“强”或“弱”),外电路中电子由N(填M或N)极流向M(填M或N)极.
分析 (1)用原电池原理设计装置比较M、N 的金属性强弱,负极金属活泼,正极上有气泡冒出;
(2)实验时,M上有气泡,N上没气泡,则M为正极,金属性M<N,金属性越强,最高价氧化物对应的水化物的碱性越强;原电池中电子由负极流向正极.
解答 解:(1)用原电池原理设计装置比较M、N 的金属性强弱,负极金属活泼,正极上有气泡冒出,则M、N作电极、稀硫酸为电解质溶液,装置图为 ,
,
故答案为: ;
;
(2)实验时,M上有气泡,N上没气泡,则M为正极,金属性M<N,可知M的最高价氧化物对应的水化物的碱性比N的最高价氧化物对应的水化物的碱性弱,外电路中电子由N流向M,故答案为:弱;N;M.
点评 本题考查原电池的设计及工作原理,为高频考点,把握金属性比较与原电池中电极判断为解答的关键,侧重分析、实验能力的考查,题目难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
15.下列物质属于同系物的一组是( )
| A. | CH4与C2H4 | |
| B. | CH3-CH=CH-CH3 与 CH3-CH2-CH2-CH3 | |
| C. | O2与O3 | |
| D. | C2H6与C3H8 |
2.某课外兴趣小组对H2O2的分解速率做了如下实验探究:
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用l0mL H2O2制取150mL O2所需的时问(s)
①验证影响反应速率的因素时要考试控制变量.取相同浓度的H2O2进行实验,上表反应条件中考虑控制单因子变量的是温度、浓度、催化剂.
②对照反应条件a和b,可以说明催化剂 因素对过氧化氢分解的速率有影响,该影响可具体表述为催化剂加快分解速率.
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试.测试结果加下.
①写出加入MnO2后H2O2发生反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②上述实验中,使用粉末状催化剂和块状催化剂所得过氧化氢分解反应的反应速率之比为10:1.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用l0mL H2O2制取150mL O2所需的时问(s)
| 浓度 时间(s) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热(t1℃) | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热(t2℃) | 360(a) | 480 | 540 | 720 |
| MnO2催化剂、加热(t2℃) | 10(b) | 25 | 60 | 120 |
②对照反应条件a和b,可以说明催化剂 因素对过氧化氢分解的速率有影响,该影响可具体表述为催化剂加快分解速率.
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试.测试结果加下.
| 催化剂(MnO2) | 操作情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 | 3min |
| 块状 | 反应较慢,火星红亮但木条未复燃 | 30min |
②上述实验中,使用粉末状催化剂和块状催化剂所得过氧化氢分解反应的反应速率之比为10:1.
16.常温下,盐酸和一元碱MOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断正确的是( )
| 实验编号 | 起始浓度/(mol•L-1) | 反应后溶液的pH | |
| c(HCl) | c(MOH) | ||
| ① | 0.1 | 0.1 | 5 |
| ② | 0.2 | x | 7 |
| ③ | 0.1 | 0.2 | 10 |
| ④ | 0.2 | 0.1 | y |
| A. | 实验①反应后的溶液中:c(MOH)约为1×10-5 mol•L-1 | |
| B. | 实验②反应后的溶液中:c(MOH)>c(M+)=c(Cl-)>c(H+)=c(OH-) | |
| C. | 实验③反应后的溶液中:c(M+)+c(H+)=c(OH-)+c(MOH) | |
| D. | 实验④反应后的溶液中:c(H+)-c(OH-)-c(MOH)=0.05mol•L-1 |
17.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
| A. | C14H18O5 | B. | C14H16O4 | C. | C16H22O5 | D. | C16H20O5 |
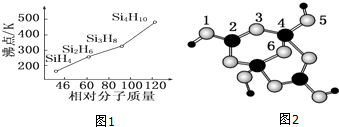
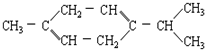 还可以简写为
还可以简写为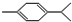 ,下列有机物中,与上述有机物互为同分异构体的是( )
,下列有机物中,与上述有机物互为同分异构体的是( )