题目内容
19.北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的球碳盐K3C60.实验测知该物质属于离子晶体,具有良好的超导性.下列关于K3C60的组成和结构分析不正确的是( )| A. | K3C60中既有离子键又有非极性键 | |
| B. | 1mol K3C60中含有的离子数目为3NA | |
| C. | 该晶体在熔融状态下能导电 | |
| D. | 该物质的化学式不能写作KC20 |
分析 A.一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键;
B.1mol K3C60中含有3mol钾离子、1mol阴离子;
C.含有自由移动离子或电子的物质能导电;
D.化学式表示该物质的组成.
解答 解:A.K3C60是离子化合物,阴阳离子之间存在离子键,C原子之间存在非极性共价键,故A正确;
B.1mol K3C60中含有3mol钾离子、1mol阴离子,所以1mol K3C60中含有的离子数目为4NA个,故B错误;
C.该物质是离子化合物,为电解质,在熔融状态下能电离出阴阳离子而导电,故C正确;
D.化学式表示该物质的组成,其化学式为K3C60,不能写为KC20,故D正确;
故选B.
点评 本题以信息给予为载体考查了离子化合物,为高频考点,明确该物质的构成微粒结合物质导电的原因来分析看到,题目难度不大.

练习册系列答案
相关题目
9.氢气可以在氧气中燃烧.在该反应中:断裂1mol H-H键消耗的能量为Q1kJ,断裂1mol O=O键消耗的能量为Q2kJ,形成1mol H-O键释放的能量为Q3 kJ.下列关系式中,正确的是( )
| A. | 2Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
10.下列说法中不正确的是( )
| A. | 19世纪中叶,门捷列夫的突出贡献是发现元素周期律 | |
| B. | 在金属和非金属元素交界处最容易找到半导体材料 | |
| C. | 在过渡元素中容易找到各种优良的催化剂和耐高温、耐腐蚀的合金材料 | |
| D. | 根据硼在元素周期表中的位置,推测硼的最高价含氧酸的化学式可能是HBO3 |
7.某学生为了探究锌与盐酸反应过程中的速率变化.在100mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如表:
(1)解释2min~3min反应速率最大的原因该反应是放热反应,2min~3min时溶液温度最高,反应速率最快;反应速率最小的时间段是4min~5min,原因为此时反应物的浓度最小,反应速率最慢.
(2)在4min~5min时间段内,用盐酸的浓度变化表示的反应速率为0.02mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A.Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是A、C、D.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50.0 | 120.0 | 232.0 | 290.0 | 312.4 |
(2)在4min~5min时间段内,用盐酸的浓度变化表示的反应速率为0.02mol•L-1•min-1.
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入下列溶液:
A.Na2CO3溶液 B.Na2SO4溶液 C.NaNO3溶液 D.少量CuSO4溶液
你认为不可行的是A、C、D.
14.氡(${\;}_{86}^{222}$Rn)可从矿泉水、岩石、地下水、天然气、建筑材料中源源不断地释放出来.它可通过呼吸进入人体,停留在呼吸道中,放出α射线,其衰变产物还能放出β、γ射线.这些射线可诱发肺癌.关于氡的下列叙述不正确的是( )
| A. | Rn的原子核内中子数与质子数的差值为50 | |
| B. | Rn位于元素周期表中第六周期0族 | |
| C. | Rn的最外层电子排布式为6s26p6,化学性质不活泼 | |
| D. | 新铺大理石地面的居室,不用打开门窗换气,因为氡对人体无危害 |
4.高温下,炽热的铁与水蒸气在一个密闭的容器中进行反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
| A. | 把铁块换成铁粉 | |
| B. | 将容器的体积压缩至原体积的一半 | |
| C. | 若保持压强不变,充入氮气使容器的体积增大 | |
| D. | 若保持体积不变,充入氮气使容器内的压强增大 |
8.反应2A(g)?2B(g)+C(g)△H>0,达平衡时,要使v(正)增大、c(A) 降低,应采取的措施是( )
| A. | 加压 | B. | 加催化剂 | C. | 降温 | D. | 升温 |
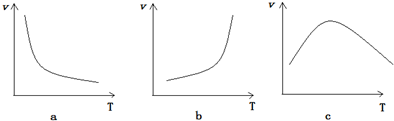
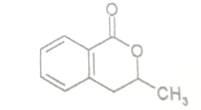
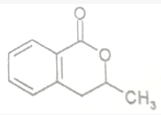 +H2O$\stackrel{NaOH}{→}$
+H2O$\stackrel{NaOH}{→}$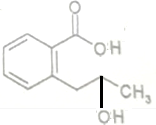 .
.