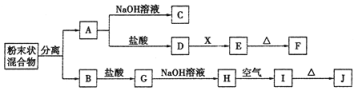
��Ŀ����
����Ŀ������������⣺
(1)10Be��9Be______________��
a����ͬһ��ԭ�ӡ�������b��������ͬ��������
c��������ͬ�Ļ�ѧ���� d��������ͬ�ĺ�������Ų�
(2)�������������ʣ�
��![]() O��
O��![]() O��
O��![]() O����H2O��D2O����ʯī�����ʯ ��H2��D2��T2����H��D��T����
O����H2O��D2O����ʯī�����ʯ ��H2��D2��T2����H��D��T����![]() K��
K��![]() Ca��
Ca��![]() Ar���ش��������⣺
Ar���ش��������⣺
a����Ϊͬλ�ص���______________��
b����Ϊͬ�����������______________��
c���ɢٺ͢��е����ܽ�ϳ�ˮ���ɵ�ˮ���ӵ�����Ϊ__________�֣��ɵ���Է���������ͬ��ˮ��������Ϊ__________�֣���Է�������������____________(д��ѧʽ)��
(3)![]() H2
H2![]() O��Ħ������Ϊ____________����ͬ������
O��Ħ������Ϊ____________����ͬ������![]() H2
H2![]() O��
O��![]() H2
H2![]() O����������֮��Ϊ______��������֮��Ϊ__________��
O����������֮��Ϊ______��������֮��Ϊ__________��
(4)�����ͬ������![]() H2
H2![]() O��
O��![]() H2
H2![]() Oʱ������������ͬ��ͬѹ�����֮��Ϊ__________������֮��Ϊ__________��
Oʱ������������ͬ��ͬѹ�����֮��Ϊ__________������֮��Ϊ__________��
���𰸡�cd �٢� �� 18 7 TO 20 g��mol��1 11��10 11��12 10��9 5��9
��������
��1��10Be��9Be��Ϊͬλ�أ����ǵ���������ͬ������������������ͬ������ͬһ��ԭ�ӣ��������Ƕ���BeԪ�ص�ԭ�ӣ���ѧ������ͬ��������ͬ�ĺ�������Ų�����ѡcd��
��2����![]() O��
O��![]() O��
O��![]() O������ԭ������������8����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
O������ԭ������������8����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
��H2O��D2O�����Dz���ԭ�ӣ�Ҳ���ǵ��ʣ�����ͬλ�ػ�ͬ����������о����룻
��ʯī�����ʯ����̼Ԫ�صĵ��ʣ���Ϊͬ�������壻
��H2��D2��T2�ֱ���![]() ��
��![]() ��
��![]() �γɵ��������ʣ����Dz���ԭ�ӣ�ȴ��ͬһ�����ʣ��������Dz���ͬλ�ػ�ͬ����������о����룻
�γɵ��������ʣ����Dz���ԭ�ӣ�ȴ��ͬһ�����ʣ��������Dz���ͬλ�ػ�ͬ����������о����룻
��H��D��T�ֱ���![]() ��
��![]() ��
��![]() �����ǵ�����������1����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
�����ǵ�����������1����������ͬ�����Ƕ�����Ԫ�ص�ͬλ�أ�
��![]() K��
K��![]() Ca��
Ca��![]() Ar�����ǵ���������ͬ���ʱ˴˲���ͬλ�أ�
Ar�����ǵ���������ͬ���ʱ˴˲���ͬλ�أ�
��a����Ϊͬλ�ص��Ǣ٢ݣ�b����Ϊͬ����������Ǣۣ�
c���ɢ٣�![]() O��
O��![]() O��
O��![]() O���͢ݣ�H��D��T���е����ܽ�ϳ�ˮ������ˮ��������������ԭ�Ӻ�һ����ԭ�ӣ�����������ԭ�ӿ����Dz�ͬ����ģ�����ԭ�ӵġ����䡱��6�֣��ʿ��γ�ˮ���ӵ�����Ϊ18��=6��3���֣��ɵ���Է���������ͬ��ˮ��������Ϊ7�֣���Է��������ֱ���18��H216O����19��HD16O��H217O����20��D216O��HT16O��HD17O��H218O����21��DT16O��D217O��HT17O��HD18O����22��T216O��DT17O��D218O��HT18O����23��T217O��DT18O����24��T218O������Է�������������T218O��
O���͢ݣ�H��D��T���е����ܽ�ϳ�ˮ������ˮ��������������ԭ�Ӻ�һ����ԭ�ӣ�����������ԭ�ӿ����Dz�ͬ����ģ�����ԭ�ӵġ����䡱��6�֣��ʿ��γ�ˮ���ӵ�����Ϊ18��=6��3���֣��ɵ���Է���������ͬ��ˮ��������Ϊ7�֣���Է��������ֱ���18��H216O����19��HD16O��H217O����20��D216O��HT16O��HD17O��H218O����21��DT16O��D217O��HT17O��HD18O����22��T216O��DT17O��D218O��HT18O����23��T217O��DT18O����24��T218O������Է�������������T218O��
��3��![]() H2
H2O��Ħ������Ϊ[(2��2)+16]g��mol-1=20g��mol-1��M(
![]() H2
H2![]() O)=22g��mol-1��1��
O)=22g��mol-1��1��![]() H216O���Ӻ�10�����Ӻ�10�����ӣ�1��
H216O���Ӻ�10�����Ӻ�10�����ӣ�1��![]() H218O���Ӻ�10�����Ӻ�12�����ӣ�����
H218O���Ӻ�10�����Ӻ�12�����ӣ�����![]() H216O��
H216O��![]() H218O����1g����1g��
H218O����1g����1g��![]() H216O��1g��
H216O��1g��![]() H218O����������Ϊ(
H218O����������Ϊ(![]() ):(
):(![]() )=11:10����������Ϊ(
)=11:10����������Ϊ(![]() ):(
):(![]() )=11:12��
)=11:12��
��4������![]() H2
H2![]() O��
O��![]() H2
H2![]() O����1g��M(
O����1g��M(![]() H2
H2![]() O)=18g��mol-1��M(
O)=18g��mol-1��M(![]() H2
H2![]() O)=20g��mol-1����n(
O)=20g��mol-1����n(![]() H2
H2![]() O)=
O)=![]() mol��n(
mol��n(![]() H2
H2![]() O)=
O)=![]() mol�������������n(
mol�������������n(![]() H2)=
H2)=![]() mol��n(
mol��n(![]() H2)=
H2)=![]() mol�����ݰ����ӵ����ɿ�֪������������ͬ��ͬѹ�µ����Ϊ
mol�����ݰ����ӵ����ɿ�֪������������ͬ��ͬѹ�µ����Ϊ![]() ��
��![]() =10��9��������Ϊ(
=10��9��������Ϊ(![]() ��2):(
��2):(![]() ��4)=5:9��
��4)=5:9��

 Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д� Ŀ�����ϵ�д�
Ŀ�����ϵ�д�����Ŀ����ѧ�������������ء�������������Ѫ�쵰�ס����쵰����O2��ϻ��Ƶ�����о����ٶ��价���¶Ⱦ�Ϊ36.8�档
(1)Ѫ�쵰��Hb���O2�γɶ���Ѫ�����ڷ�Ӧ�٣�HbH+(aq)+O2(g)![]() HbO2(aq)+H+(aq)���÷�Ӧ���Է����У�������H______0(���������)��ѪҺ�л�ͬʱ���ڷ�Ӧ�ڣ�CO2+H2O
HbO2(aq)+H+(aq)���÷�Ӧ���Է����У�������H______0(���������)��ѪҺ�л�ͬʱ���ڷ�Ӧ�ڣ�CO2+H2O![]() H++HCO3-����Ϸ�Ӧ�٢ڣ��β�����ѹ_____(��ϸߡ��ϵ͡�)������CO2�ų����⣬�ӻ�ѧƽ��ǶȽ���ԭ�� ____________��
H++HCO3-����Ϸ�Ӧ�٢ڣ��β�����ѹ_____(��ϸߡ��ϵ͡�)������CO2�ų����⣬�ӻ�ѧƽ��ǶȽ���ԭ�� ____________��
(2)�����д������쵰�� MbҲ�ɽ��O2�γ�MbO2������Ӧ�ۣ�Mb(aq)+O2(g)![]() MbO2(aq)����ƽ�ⳣ��K=
MbO2(aq)����ƽ�ⳣ��K=![]() �������������䣬��������ѹp(O2)����Kֵ___(��������С�����䡱)����֪������ѹp(O2)=2.00 kPa ��ƽ����ϵ�У�
�������������䣬��������ѹp(O2)����Kֵ___(��������С�����䡱)����֪������ѹp(O2)=2.00 kPa ��ƽ����ϵ�У�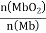 =4.0������Ŀ�����p(O2)=21 kPa�������ʱ Mb������������϶�(ƽ��ת����)ԼΪ_______________(������λ��Ч����)��
=4.0������Ŀ�����p(O2)=21 kPa�������ʱ Mb������������϶�(ƽ��ת����)ԼΪ_______________(������λ��Ч����)��
(3)Hb���Ӿ����ĸ��ǻ�����ÿ���ǻ������ֹ���(T�ͺ�R��)��ͼ�У�T0��R0��ʾδ���O2��T�ͺ�R�ͣ��Ҵ��ڿ���ı乹ЧӦ��T0![]() R0������ƽ�ⳣ��ΪK0�����ķ���O2��Hb���ĸ��ǻ���Ϻ�T4
R0������ƽ�ⳣ��ΪK0�����ķ���O2��Hb���ĸ��ǻ���Ϻ�T4![]() R4Ҳ�DZ乹ЧӦ������ƽ�ⳣ��ΪK4��
R4Ҳ�DZ乹ЧӦ������ƽ�ⳣ��ΪK4��
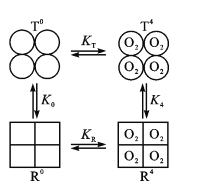
����֪ij���ײ��˷�����T0+4O2![]() T4��Ӧ��n(O2)�������£�
T4��Ӧ��n(O2)�������£�
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n(O2)/10-6 mol | 1.68 | 1.64 | 1.58 | 1.50 | 1.40 |
����2.0 min~8.0 min����T�����ʵ����仯��ʾ�ķ�Ӧ����v(T4)Ϊ_________mol��min-1��
���ּٶ�R��Hb��O2�Ľ�ϳ���ΪKR��T��Hb��O2�Ľ�ϳ���ΪKT����֪KR��KT����ͼ��K0____K4(���������)��
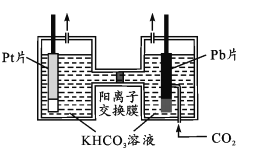
(4)������������ز����ٵ����ʡ�����ͼ��ʾ����PtΪ������Pb(CO2)�����壬ʹCO2�Ϊ��������⾭CO2���ʹ�����KHCO3��Һ��ʹ����������ͬʱ�õ��״�����������ӦʽΪ____���ӵ�����Һ�з���״��IJ���������_______________��