��Ŀ����
����Ŀ��A��H�ֱ��ʾ��ѧ��ѧ�г�����ij�����ʣ�����֮����ת����ϵ����ͼ��ʾ(���ַ�Ӧ�������δ�г�)����֪��C��D��E��F��G���������о�����ͬһ��Ԫ�أ�AΪ����ɫ���廯���GΪ���ɫ���塣

(1)д����ѧʽ��A��________________��C��________________��F��________________��
(2)д����Ӧ�Ļ�ѧ����ʽ��
��_____________________________________________________________��
��_____________________________________________________________��
(3)д�����ӷ���ʽ��
��_____________________________________________________________��
��_____________________________________________________________��
(4)����24 g B��Ҫת��________mol���ӡ�
���𰸡�Na2O2Fe3O4Fe(OH)22O2��3Fe![]() Fe3O44Fe(OH)2��O2��2H2O===4Fe(OH)3Fe3O4��8H��===Fe2����2Fe3����4H2OFe3����3OH��===Fe(OH)3��1.5
Fe3O44Fe(OH)2��O2��2H2O===4Fe(OH)3Fe3O4��8H��===Fe2����2Fe3����4H2OFe3����3OH��===Fe(OH)3��1.5
��������
C��D��E��F��G�о�����ͬһ��Ԫ�أ�GΪ���ɫ���壬��D��OH-��Ӧ����F��F�ڿ����з������ɵ�G�����ж�GΪFe(OH)3��FΪFe(OH)2��D�Ǻ����������ӵĿ������Ρ�AΪ����ɫ���廯���AΪNa2O2��BΪO2��HΪNaOH��H��E��Ӧ����G����E�Ǻ��������ӵĿ������Ρ�Cת��ΪD��E��Bת��ΪC����C��������������D������FeCl2��E������FeCl3���ݴ˽��
�������Ϸ�����֪AΪNa2O2��BΪO2��C��������������D������FeCl2��E������FeCl3��FΪFe(OH)2��GΪFe(OH)3��HΪNaOH����
��1��A��C��F�Ļ�ѧʽ�ֱ���Na2O2��Fe3O4��Fe(OH)2��
��2����Ӧ�ڵķ���ʽΪ2O2��3Fe![]() Fe3O4����Ӧ�ķ���ʽΪ4Fe(OH)2��O2��2H2O��4Fe(OH)3��
Fe3O4����Ӧ�ķ���ʽΪ4Fe(OH)2��O2��2H2O��4Fe(OH)3��
��3����Ӧ�۵����ӷ���ʽΪFe3O4��8H����Fe2����2Fe3����4H2O����Ӧ�ݵ����ӷ���ʽΪFe3����3OH����Fe(OH)3����
��4������B�ķ�ӦΪ2Na2O2+2H2O��4NaOH+O2����������������Ϊ-1�ۣ���������Ϊ0�ۣ���ÿ����1molO2ת��2mol���ӣ�������24g���������������ʵ�����24g��32g/mol��0.75mol����ת�Ƶ��ӵ����ʵ�����0.75mol��2��1.5mol��

 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�����Ŀ��H2O2��һ�ֳ����Լ�����ʵ���ҡ���ҵ�������й㷺��;

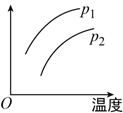
��.ʵ������H2O2������������ֽ������ܶ�������Ӱ�졣ʵ����70��ʱ��ͬ������H2O2Ũ����ʱ��ı仯����ұ�����ͼ��ʾ��
��1������˵����ȷ���ǣ�________������ĸ��ţ�
A��ͼ�ױ���������������ͬʱ��H2O2Ũ��ԽС����ֽ�����Խ��
B��ͼ�ұ���������������ͬʱ����Һ����Խ����H2O2�ֽ�����Խ��
C��ͼ������������Mn 2+����ʱ����Һ����Խǿ��H2O2�ֽ�����Խ��
D��ͼ����ͼ��������������Һ�У�Mn2+��H2O2�ֽ����ʵ�Ӱ���
��2������Mn2+�ڷ�Ӧ�У��ı���____________________(����ĸ���)
A����Ӧ���� B����Ӧ��C����Ӧ�ʱ� D����Ӧ·��
E.��Ӧ��� F.����Ӱٷ���
��. H2O2�ڹ�ҵ����ΪFenton����Ҫ�Լ��������ڴ������ѽ����л���Ĺ�ҵ��ˮ���ڵ��ں�pH����Һ������ԣ���Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�졣
��ʵ����ơ�����p-CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298K��313K������ʵ���������±�����������¶Ա����飬����ʵ��������ʱ��-p-CPŨ��ͼ���¡�

��3�������Ե��ǻ����ɻ��ĵ���ʽΪ��______________
��4�����������ʵ����Ʊ�(���в�Ҫ���ո�)��
ʵ�� ��� | ʵ��Ŀ�� | T/K | pH | c/10-3mol��L-1 | |
H2O2 | Fe2+ | ||||
�� | Ϊ����ʵ�����ο� | 298 | 3 | 6.0 | 0.30 |
�� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | _________ | ______ | _______ | _________ |
�� | __________________ | <>298 | 10 | 6.0 | 0.30 |
��5�����������ͼʵ�������ߣ����㽵�ⷴӦ��50��150s�ڵķ�Ӧ���ʣ�v(p-CP)=_____________
��6��ʵ��ʱ���ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еķ�Ӧ����ֹͣ����������ʵ����������һ��Ѹ��ֹͣ��Ӧ�ķ�����__________________________��