题目内容
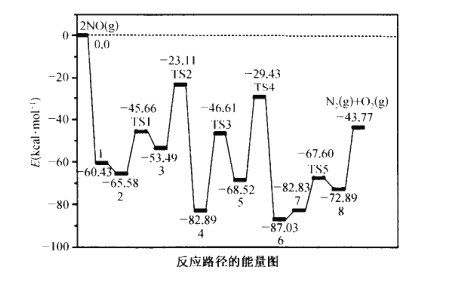
【题目】NO在催化剂表面催化分解反应历程如图所示(TS表示反应中的过渡态)。下列有关说法中正确的是
A.分解反应的热化学方程式为 2NO(g)![]() N2(g)+O2(g)△H = +43.77 kcal mol-1
N2(g)+O2(g)△H = +43.77 kcal mol-1
B.中间产物3中的键能大于中间产物4的,中间产物3更稳定
C.历程中“5→TS4→6”的活化能最大,该历程决定整个反应的快慢
D.使用高效催化剂,降低NO的相对能量,从而影响反应热的大小
【答案】C
【解析】
A.由图像可知,反应物的总能量高于生成物的总能量,反应为放热反应,则分解反应的热化学方程式为 2NO(g)![]() N2(g)+O2(g)△H = -43.77 kcal mol-1,故A错误;
N2(g)+O2(g)△H = -43.77 kcal mol-1,故A错误;
B.由图像可知,中间产物3能量高于中间产物4的能量,为放热反应,中间产物3中的键能小于中间产物4的,能量越低越稳定,则中间产物4更稳定,故B错误;
C.过渡态和反应物的能量差(△E)称为活化能,根据图示计算可得,历程中“5→TS4→6”的活化能最大,活化能越大,反应速率越慢,反应历程中慢反应决定整个反应的快慢,故C正确;
D.使用高效催化剂,可以改变反应物的活化能,但不能影响反应热,反应热由反应物的总能量和生成物的总能量决定,故D错误;
答案选C。

【题目】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。某同学以含铜废料(主要成分是 CuO、MgO、MnO、SiO2及少量的杂质)为主要原料制备CuCl的主要流程如下:

已知:①CuCl难溶于水和乙醇 ,在潮湿的空气中易被氧化;
②在水溶液中存在平衡 :CuCl(白色)+2Cl-![]() [CuCl3]2-(色无溶液)。
[CuCl3]2-(色无溶液)。
③几种金属氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | 开始沉淀的 pH | 完全沉淀的 pH |
Mg(OH)2 | 8. 4 | 10. 8 |
Cu(OH)2 | 4.2 | 6. 7 |
Mn(OH)2 | 7. 8 | 8. 8 |
问答下列问题:
(1)滤渣1 的主要成分是 _________________(写化学式,下同)。
(2)“调pH”所用粉末状试剂 X 是_____________;pH的调节范闱为____________。
(3)“反应”发生 Cu2+ +Cu+6Cl-=2[CuCl3]2-,表明已完全反应的现象是_______________。
(4)向“滤液3” 加大量的水,过滤可得 CuCl。所得沉淀需再用乙醇洗涤.并在低温下干燥,其原因是___________。
(5)产品纯度的测定,步骤如下:称取mg试样置于锥形瓶中,加入直径 4 ~ 5 mm 玻璃珠适量,并加入 10 mL FeCl3溶液,摇动至样品全部溶解后(CuCl+FeCl3=CuCl2+FeCl2),再加入50 mL,水和2滴邻菲罗啉指示剂,立刻用c mol L-1 的硫酸高铈[Ce(SO4)2]标准溶液滴定(Fe2++Ce4+=Fe3++Ce3+)'滴至终点时共消耗硫酸高铈标准溶液V mL。
①锥形瓶中加入玻璃珠的作用是____________________。
②样品中 CuCl 的质量分数为_____(列出表达式即可 , 用含(c、m、V的代数式表示)。