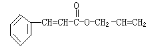题目内容
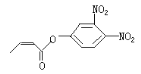
【题目】“达菲”是瑞士罗氏公司研制的有效治疗人类禽流感的药物。达菲的主要合成原料是我国盛产的莽草酸。


下列说法不正确的是( )
A.莽草酸可溶于水
B.1 mol莽草酸最多可和4 molNaOH溶液反应
C.从结构上推测,达菲既可与盐酸反应又可与氢氧化钠溶液反应
D.从结构上推测,以莽草酸为原料合成达菲须经过酯化反应等步骤
【答案】B
【解析】
试题分析:A. 莽草酸中含有羟基和羧基,属于亲水基团,因此可溶于水,A正确;B. 1 mol莽草酸中含有3mol醇羟基和1mol羧基,醇羟基与NaOH溶液不反应,羧基能与NaOH溶液反应,因此最多可消耗NaOH溶液1mol,B错误;C.从结构上看,达菲中含有酯基和氨基,含有酯基可在NaOH溶液中发生碱性水解,含有氨基可与盐酸反应,因此达菲既可与盐酸反应,又可与氢氧化钠溶液反应,C正确;D. 莽草酸中含有羧基,达菲中含有酯基,因此从结构上推测,以莽草酸为原料合成达菲须经过酯化反应等步骤,D正确。故答案B。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | ||||||||||||||||
c | d | e | |||||||||||||||
f | g | ||||||||||||||||
试回答下列问题(凡涉及的物质均用化学式表示):
(1)a的氢化物的分子构型为 ,中心原子的杂化形式为 ;d的最高价氧化物的分子构型为 ,中心原子的杂化形式为 ,该分子是 (填“极性”或“非极性”)分子。
(2)b、d、e三种元素的氢化物中的沸点最高的是 ,原因是: 。
(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式(必须将配位键表示出来) 。
(4)f(NH3)5BrSO4可形成两种配合物 ,已知f3+ 的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为 ,该配合物的配体是 、 ;