题目内容
16.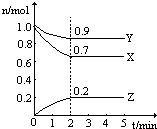 在一定条件下,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
在一定条件下,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:(1)从开始至2min,Z的平均反应速率为0.05mol/(L•min);
(2)该反应的化学方程式为3X+Y?2Z.
分析 (1)分析图象计算Z的物质的量增加量为0.2mol,结合反应速率概念计算,V=$\frac{△c}{△t}$;
(2)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式.
解答 解:(1)图象计算Z的物质的量增加量为0.2mol,从开始至2min,Z的平均反应速率=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L•min);
故答案为:0.05mol/(L•min);
(2)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y?2Z,
故答案为:3X+Y?2Z.
点评 本题考查了化学反应速率,化学方程式的书写及应用,图象分析速率之比等于对应物质的计量数之比是解题关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.以下用于研究有机物的方法错误的是( )
| A. | 蒸馏用于分离液态有机混合物 | |
| B. | 燃烧法是研究有机物成分的一种有效方法 | |
| C. | 核磁共振氢谱通常用于分析有机物的相对分子质量 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
7.下列各组粒子中,互为同位素的是( )
| A. | O2和O3 | B. | SO2和SO3 | C. | 12C和13C | D. | D2O和T2O |
4.关于主族元素的叙述,不正确的是( )
| A. | 元素原子的最外层电子数等于主族族序数 | |
| B. | 元素的最高价等于原子最外层电子数 | |
| C. | 最低负价数的绝对值等于原子最外层变稳定结构时所需电子数 | |
| D. | 同周期元素原子具有相同的核外电子层数 |
1.下列说法正确的是( )
| A. | 化学反应中的能量变化均表现为热量的变化 | |
| B. | 化学键的断裂和形成是化学反应中的能量变化的主要原因 | |
| C. | 需要加热才能够发生的反应一定是吸热反应 | |
| D. | 在一个确定的化学反应过程中,反应物的总能量总是高于生成物的总能量 |
5.可逆反应2NO2?2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ( )
①单位时间内生成n mol O2 的同时生成2n mol NO2
②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态.
①单位时间内生成n mol O2 的同时生成2n mol NO2
②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态.
| A. | ①③ | B. | ②③④ | C. | ②③ | D. | ①④ |
19. 物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )
物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )
 物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )
物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )| A. | X分子式为C6H7O7 | |
| B. | 1 mol物质X可以和4mol氢氧化钠发生反应 | |
| C. | X分子内所有原子均在同一平面内 | |
| D. | 足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同 |
 原电池是一种将化学能转化为电能的装置.在Cu-Zn原电池中,Zn极是电池的负极(填“正极”或“负极”)发生氧化反应(填“氧化”或“还原”),电极反应式为Zn-2e-=Zn2+.
原电池是一种将化学能转化为电能的装置.在Cu-Zn原电池中,Zn极是电池的负极(填“正极”或“负极”)发生氧化反应(填“氧化”或“还原”),电极反应式为Zn-2e-=Zn2+.