题目内容
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物。
(1)下列叙述正确的是 。(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个 键和1个大
键和1个大 键,C6H6是非极性分子
键,C6H6是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
Mn元素价电子排布式为 ,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是 。
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。
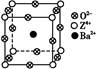
(4)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为 。

(5)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
①H、C、N、O四种元素的电负性由小到大的顺序为 。
②与CNO-互为等电子体微粒的化学式为 (写出一种即可)。
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(1)下列叙述正确的是 。(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个
 键和1个大
键和1个大 键,C6H6是非极性分子
键,C6H6是非极性分子D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
| 元 素 | Mn | Fe | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn元素价电子排布式为 ,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是 。
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。
(4)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为 。

(5)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
①H、C、N、O四种元素的电负性由小到大的顺序为 。
②与CNO-互为等电子体微粒的化学式为 (写出一种即可)。
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(1) A D 2分 (2)3d54s2 2分 Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态。) 2分 (3)d区 1分 (4) TiO2 2分
(5)① H<C<N<O 2分 ②CO2(N2O)、SCN-2分 ③ N≡C—O—H 2分
(5)① H<C<N<O 2分 ②CO2(N2O)、SCN-2分 ③ N≡C—O—H 2分
试题分析:(1)A、由于氧元素的电负性大,所以CH2O与水分子间能形成氢键,A正确;B、CH2O分子是平面型结构,中心原子碳原子是sp2杂化,CO2分子是直线型结构,中心原子碳原子采用sp杂化,B不正确;C、C6H6结构是正六边形结构,属于非极性分子。C6H6分子中碳原子是sp2杂化,其中每个碳原子与碳原子形成2个σ键,与氢原子形成1个σ键,所以共含有12个σ键和1个大π键,C不正确;D、CO2晶体是分子晶体,而二氧化硅晶体是原子晶体,所以CO2的熔点、沸点都比二氧化硅晶体的低,D正确,答案选AD。
(2)Mn是25号元素,则根据核外电子排布规律可知,Mn元素价电子排布式为3d54s2;由于Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态(或Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态。),所以气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。
(3)区的名称来自于安装构造原理最后填入电子的轨道名称,Ti是22号元素,其价电子排布式为3d24s2,所以Ti元素位于d去。
(4)根据晶胞结构可知,氧原子位于面心处与晶胞内,Ti原子位于顶点处和体心处,所以根据均摊原理可知,结构中氧原子的个数=4×
 +2=4个,Ti原子个数=1+8×
+2=4个,Ti原子个数=1+8× =2,所以化学式为TiO2。
=2,所以化学式为TiO2。(5)①非金属性越强,电负性越小。因此同周期自左向右电负性逐渐增大,则H、C、N、O四种元素的电负性由小到大的顺序为H<C<N<O。
②价电子数与原子数分别都相等的互为等电子体,则与CNO-互为等电子体微粒的化学式为CO2(N2O)、SCN-等。
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,因此分子中C与N形成三键,其余均是单键,所以氰酸的结构式N≡C—O—H。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目

 为碳原子,
为碳原子, 为硅原子)。每个碳原子周围与其距离最近的硅原子有________个。设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。
为硅原子)。每个碳原子周围与其距离最近的硅原子有________个。设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为________(用含a、b的式子表示)。
 的空间构型为 ,与其互为等电子体的一种分子为 。
的空间构型为 ,与其互为等电子体的一种分子为 。 
 (一)在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(一)在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。


