题目内容
【题目】最近,科学家研发了“全氢电池”,其工作原理如图所示。下列有关该电池工作时的说法,正确的是( )
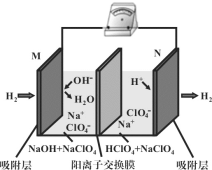
A. 电解质溶液中,Na+向左移动
B. 该电池的总反应为H+ + OH- = H2O
C. 电子由N电极经导线流向M电极
D. 导线上通过1mole-,装置内H2总量减少0.5mol
【答案】B
【解析】
由图可知,N电极上H+得电子被还原成H2,M电极上H2失电子发生氧化反应生成H2O,则左边M电极是负极,右边N电极是正极。
A. 根据以上分析,左边M电极是负极,右边N电极是正极,则电解质溶液中,由于阳离子向正极移动,所以Na+向右移动,故A错误;
B. 负极的电极反应式为H2-2e-+2OH-=2H2O,正极的电极反应式为2H++2e-=H2↑,所以总反应为H+ + OH- = H2O,故B正确;
C. 根据以上分析,左边M电极是负极,右边N电极是正极,所以电子由M电极经导线流向N电极,故C错误;
D. 由电池的总反应H+ + OH- = H2O可知,负极消耗的氢气等于正极产生的氢气,故D错误。
答案选B。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】如表为元素周期表中的一部分,表中列出了10种元素在周期表中的位置,按要求完成下列各小题。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | Ⅵ A | Ⅶ A | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
I.(1)这10种元素中,化学性质最不活泼的元素是____(填元素符号,下同),非金属性最强的元素是___。
(2)①③⑤三种元素的最高价氧化物对应的水化物中,碱性最强的化合物的电子式是
(3)①②③三种元素的原子半径由大到小的顺序是____。
(4)某元素的最高价氧化物对应的水化物既能与酸反应生成盐和水又能和碱反应生成盐和水,向该元素和⑨号元素形成的化合物的溶液中,缓慢滴加氢氧化钠溶液至过量,产生的实验现象是____,有关反应的离子方程式为_____。
II.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩Ar
(1)既含有极性键又含有非极性键的是____;(填序号,下同)
(2)含有非极性键的离子化合物是____;
(3)不含化学键的是____;
(4)用电子式表示Na2O的形成过程_____。