题目内容
11.X22-离子共有2n个电子,元素X的原子核内的质子数为( )| A. | n-1 | B. | n+1 | C. | n | D. | 2n |
分析 阴离子核外电子数=质子数-离子所带电荷.
解答 解:设X的质子数为Z,则2Z-(-2)=2n,故Z=n-1,故选:A.
点评 本题考查质子数、电子数与电荷数关系,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.下列叙述错误的是( )
| A. | 将10gNaCl晶体溶入90g水中,制得10%的NaCl溶液 | |
| B. | 将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L | |
| C. | 将wga%的NaCl溶液蒸发掉$\frac{w}{2}$g水,得到2a%的NaCl溶液 | |
| D. | 将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2 c1mol/L |
19.下列金属活动性最强的( )
| A. | Mg | B. | Ag | C. | Cu | D. | Zn |
6.已知25℃时,醋酸、碳酸、次氯酸、氢氟酸和亚硫酸的电离平衡常数分别为
(1)写出H2SO3的电离方程式H2SO3?H++HSO3-,HSO3-?H++SO32-.
(2)在25℃时,相同物质量浓度、相同体积的上述五种酸溶液中,氢离子浓度最大的是H2SO3(填“醋酸”、“碳酸”、“次氯酸”、“氢氟酸”或“亚硫酸”,下同);水电离的氢离子浓度最大的是HClO.
(3)在25℃时,0.1mol•L-1的氢氟酸的电离度=6%;溶液pH的测定可用广泛pH试纸,其操作方法是:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有HF溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较,确定溶液的pH;加水稀释该氢氟酸溶液,下列数值增大的是BD.
A.c(F-) B.c(OH-) C.c(H+)•c(OH-) D.c(F-)/c(HF) E.c(F-)/c(HF)•c(OH-)
(4)下列离子方程式中正确的是AC.
A.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-═HCO3-+HClO
B.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO
C.过量SO2通入碳酸钠溶液中:2SO2+H2O+CO32-═2HSO3-+CO2
D.过量CH3COOH加入碳酸钠溶液中:CH3COOH+CO32-═CH3COO-+HCO3-
(5)若反应反应:Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增加,可以加入E.
A.Na2SO3 B.H2O C.Na2CO3D.NH3•H2OE.NaHCO3
(6)常温下,0.1mol/L醋酸溶液与0.01mol/L醋酸溶液中的c(H+)分别为A与B,则两者的c(H+)大小关系为:A小于10B.(填“大于”、“等于”、“小于”)
| 弱电解质 | CH3COOH | HClO | HF | H2CO3 | H2SO3 |
| 电离平衡常数 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka=3.6×10-4 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.5×10-2 Ka2=1.0×10-7 |
(2)在25℃时,相同物质量浓度、相同体积的上述五种酸溶液中,氢离子浓度最大的是H2SO3(填“醋酸”、“碳酸”、“次氯酸”、“氢氟酸”或“亚硫酸”,下同);水电离的氢离子浓度最大的是HClO.
(3)在25℃时,0.1mol•L-1的氢氟酸的电离度=6%;溶液pH的测定可用广泛pH试纸,其操作方法是:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有HF溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较,确定溶液的pH;加水稀释该氢氟酸溶液,下列数值增大的是BD.
A.c(F-) B.c(OH-) C.c(H+)•c(OH-) D.c(F-)/c(HF) E.c(F-)/c(HF)•c(OH-)
(4)下列离子方程式中正确的是AC.
A.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-═HCO3-+HClO
B.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO
C.过量SO2通入碳酸钠溶液中:2SO2+H2O+CO32-═2HSO3-+CO2
D.过量CH3COOH加入碳酸钠溶液中:CH3COOH+CO32-═CH3COO-+HCO3-
(5)若反应反应:Cl2+H2O?HCl+HClO达到平衡后,要使HClO浓度增加,可以加入E.
A.Na2SO3 B.H2O C.Na2CO3D.NH3•H2OE.NaHCO3
(6)常温下,0.1mol/L醋酸溶液与0.01mol/L醋酸溶液中的c(H+)分别为A与B,则两者的c(H+)大小关系为:A小于10B.(填“大于”、“等于”、“小于”)
20.在强碱溶液中,可能大量存在的离子组是( )
| A. | Na+、K+、AlO2-、Cl- | B. | Ba2+、Na+、Al3+、SO42- | ||
| C. | K+、Mg2+、Cl-、NO3- | D. | Na+、Ca2+、Cl-、HCO3- |
1.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,28g CO和N2的混合气体中含有的分子总数为NA | |
| B. | 1 mol铁与足量盐酸完全反应时失去的电子数为3NA | |
| C. | 78g过氧化钠晶体中,含2NA个阴离子 | |
| D. | 标准状况下,22.4 LH2S和SO2的混合气体中含有的分子总数为NA |
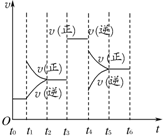 在一密闭容器中发生下列反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图所示是某一时间段中反应速率与反应进程的曲线关系.回答下列问题:
在一密闭容器中发生下列反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图所示是某一时间段中反应速率与反应进程的曲线关系.回答下列问题: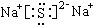 ,
,