题目内容
(1)在298K时,1mol C2H6 在氧气中完全燃烧生成CO2和液态水,放出热量1558.3kJ。写出该反应的热化学方程式 。
(2)利用该反应设计一个燃料电池:用KOH溶液作电解质溶液,多孔石墨作电极,在电极上分别通入乙烷和氧气。通入乙烷气体的电极应为 极(填“正”或“负”),该电极上发生的电极反应式为 。
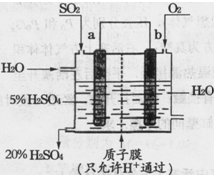
(3)在右图所示实验装置中,石墨棒上的电极反应式为 。如果起始时盛有1L pH=5的CuSO4溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 。若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 。

(4)将普通碳钢钉放入“84消毒液”(NaClO溶液)中浸泡一段时间。预期的实验现象是 。
(5)为了进一步探究碳钢钉在该消毒液(NaClO)中的腐蚀原理,某同学设计了如图所示实验装置,写出碳(C)极上发生的电极反应式 。

(2)利用该反应设计一个燃料电池:用KOH溶液作电解质溶液,多孔石墨作电极,在电极上分别通入乙烷和氧气。通入乙烷气体的电极应为 极(填“正”或“负”),该电极上发生的电极反应式为 。
(3)在右图所示实验装置中,石墨棒上的电极反应式为 。如果起始时盛有1L pH=5的CuSO4溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1,此时可观察到的现象是 。若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入 (填物质名称),其质量约为 。

(4)将普通碳钢钉放入“84消毒液”(NaClO溶液)中浸泡一段时间。预期的实验现象是 。
(5)为了进一步探究碳钢钉在该消毒液(NaClO)中的腐蚀原理,某同学设计了如图所示实验装置,写出碳(C)极上发生的电极反应式 。

(1)2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H=?3116.6 kJ·mol-1(2分)
(2)负 C2H6+18OH-?14e-=2CO32-+12H2O
(3)4OH-?4e-=2H2O+O2↑(2H2O?4e-=O2↑+4H+)
石墨电极表面有气泡产生,铁电极上附着一层红色物质,溶液颜色变浅氧化铜(或碳酸铜) 4g(或6.2g)
(4)钢钉表面有红褐色物质生成
(5)ClO-+H2O+2e-=Cl-+2OH-
(2)负 C2H6+18OH-?14e-=2CO32-+12H2O
(3)4OH-?4e-=2H2O+O2↑(2H2O?4e-=O2↑+4H+)
石墨电极表面有气泡产生,铁电极上附着一层红色物质,溶液颜色变浅氧化铜(或碳酸铜) 4g(或6.2g)
(4)钢钉表面有红褐色物质生成
(5)ClO-+H2O+2e-=Cl-+2OH-
 试题分析:(1)依据热化学方程式的书写原则结合定量关系写出反应为生成物、各物质的聚集状态、对应反应的焓变得到热化学方程式为:2 C2H6(g)+7 O2(g)→4 CO2(g)+6 H2O(l)△H=-3116.6 kJ/mol;
试题分析:(1)依据热化学方程式的书写原则结合定量关系写出反应为生成物、各物质的聚集状态、对应反应的焓变得到热化学方程式为:2 C2H6(g)+7 O2(g)→4 CO2(g)+6 H2O(l)△H=-3116.6 kJ/mol;故答案为:2 C2H6(g)+7 O2(g)→4 CO2(g)+6 H2O(l)△H="-3116.6" kJ/mol;
(2)利用反应①2 C2H6(g)+7 O2(g)→4 CO2(g)+6 H2O(l)△H="-3116.6" kJ/mol;设计原电池,根据化合价变化分析判断,乙烷失电子发生氧化反应,所以通入乙烷气体的电极应为负极,正极电极反应为:②O2+2H2O+4e-=4OH-; ①-②×7 得到负极电极反应为:C2H6-14e-+18OH-═2CO32-+12H2O;(3)如图所示实验装置中,石墨棒上是电子流出一端,电解池中电子流出的是阳极,所以阳极电极反应为氢氧根离子放电,电极反应为:4OH--4 e-═O2↑+2H2O;惰性电极电解硫酸铜溶液生成铜、氧气、硫酸,恢复原溶液浓度需要加入析出的物质,即加入氧化铜可以恢复,故答案为:4OH--4 e-═O2↑+2H2O;CuO;将碳钢铁钉浸在次氯酸钠中,会发生电化学腐蚀。其中铁为负极,碳为正极。铁失电子,因为次氯酸根离子的强氧化性,次氯酸根离子得电子生成Cl—。故(4)钢钉表面有红褐色物质生;(5)ClO-+H2O+2e-═Cl-+2OH-

练习册系列答案
相关题目
 2N (g)
2N (g) 2H (g)
2H (g)
 (3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为: 2SO3(g) △H="-197" kj/mol。开始时在10 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出197kJ的热量,该温度下的平衡常数K= ,升高温度K将 (填“增大、减小或不变”)。
2SO3(g) △H="-197" kj/mol。开始时在10 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出197kJ的热量,该温度下的平衡常数K= ,升高温度K将 (填“增大、减小或不变”)。 2SO3(g),化学兴趣小组的同学探究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出了下列关系图。下列判断中正确的是 (填字母)。
2SO3(g),化学兴趣小组的同学探究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出了下列关系图。下列判断中正确的是 (填字母)。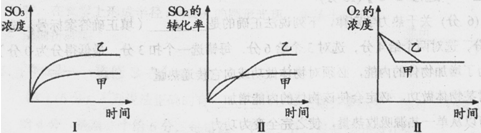


 CH3OH(g),CO的平衡转化率与温度、压强的关系如下图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如下图所示,则:



 Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol。