题目内容
已知:①溶液中CrO42—显黄色,Cr2O72-显橙红色
②PbCrO4难溶于水,也难溶于强酸
③H+(aq)+OH-(aq)=H2O(l); ΔH=" —a" KJ/mol
3Cl2(g)+2Cr3+(aq)+16OH-(aq)=2CrO42-(aq)+6Cl-(aq)+8H2O(l);ΔH="—b" KJ/mol
2CrO42-(aq)+2H+(aq) Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
平衡常数K=9.5×104 (上述a、b、c均大于0)
对上述反应⑤,取50mL溶液进行试验,部分测定数据如下:
试回答下列问题:
(1)0.02s到0.03s之间用Cr2O72-表示该反应的平均反应速率为
下列说法正确的( )
A、0.03s时V正(CrO42—)=2V逆(Cr2O72—)
B、溶液pH值不变说明该反应已达平衡状态
C、溶液中c(CrO42—):c(Cr2O72—)=2:1时该反应已达平衡状态
D、反应放热2.5×10-3c KJ时CrO42—的转化率为50%
E、升温该反应平衡常数变大
F、0.04s时加入足量的Pb(NO3)2 可使溶液由橙色变为黄色
(3)0.03s时溶液的pH=
(4)已知酸性条件下Cr2O72—将Cl-氧化为Cl2,本身被还原为Cr3+为放热反应,试写出该反应的热化学方程式:
②PbCrO4难溶于水,也难溶于强酸
③H+(aq)+OH-(aq)=H2O(l); ΔH=" —a" KJ/mol
3Cl2(g)+2Cr3+(aq)+16OH-(aq)=2CrO42-(aq)+6Cl-(aq)+8H2O(l);ΔH="—b" KJ/mol
2CrO42-(aq)+2H+(aq)
 Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol平衡常数K=9.5×104 (上述a、b、c均大于0)
对上述反应⑤,取50mL溶液进行试验,部分测定数据如下:
| 时间(s) | 0 | 0.01 | 0.02 | 0.03 | 0.04 |
| n (CrO42—)(mol) | 0.01 | 8.0×10-4 | 5.4×10-4 | 5.0×10-4 | |
| n (Cr2O72—)(mol) | 0 | | 4.73×10-3 | | 4.75×10-3 |
试回答下列问题:
(1)0.02s到0.03s之间用Cr2O72-表示该反应的平均反应速率为
下列说法正确的( )
A、0.03s时V正(CrO42—)=2V逆(Cr2O72—)
B、溶液pH值不变说明该反应已达平衡状态
C、溶液中c(CrO42—):c(Cr2O72—)=2:1时该反应已达平衡状态
D、反应放热2.5×10-3c KJ时CrO42—的转化率为50%
E、升温该反应平衡常数变大
F、0.04s时加入足量的Pb(NO3)2 可使溶液由橙色变为黄色
(3)0.03s时溶液的pH=
(4)已知酸性条件下Cr2O72—将Cl-氧化为Cl2,本身被还原为Cr3+为放热反应,试写出该反应的热化学方程式:
(1)4×10-2mol/(L?S);(2)ABD;(3)1;
(4)Cr2O72- +6Cl-+14H+=3Cl2+2Cr3++7H2O ΔH=(c+b-16a)KJ/mol
(4)Cr2O72- +6Cl-+14H+=3Cl2+2Cr3++7H2O ΔH=(c+b-16a)KJ/mol
试题分析:CrO42—的物质的量变化5.4×10-4- 5.0×10-4= 4.0×10-5 mol,用CrO42-表示的速率是8×10-2 mol/(L?S),依CrO42-(aq)+H+(aq)
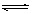 Cr2O72-可知,用Cr2O72—表示的速率是4×10-2 mol/(L?S) mol/(L?S)
Cr2O72-可知,用Cr2O72—表示的速率是4×10-2 mol/(L?S) mol/(L?S)0.03s时,CrO42—有5.4×10-4- 5.0×10-4= 4.0×10-5 mol转变成Cr2O72—,Cr2O72—增加4.0×10-5 mol,即共为4.73×10-3+4.0×10-5 mol=4.75×10-3mol,所以0.03s时是平衡状态;此时V正(CrO42—)=2V逆(Cr2O72—)。A对。溶液pH值不变说明H+浓度不变,该反应已达平衡状态;B对。平衡是c(CrO42—):c(Cr2O72—)= 5.0×10-4: 4.75×10-3,不是2:1,C错。反应放热2.5×10-3c KJ时,CrO42—转化5.0×10-3 mol ,CrO42—的转化率为5.0×10-3 mol÷0.01mol =50%,D正确。该反应时放热反应,升温该反应平衡常数变小,E错误。0.04s时是平衡状态,由于PbCrO4难溶于水,也难溶于强酸,加入足量的Pb(NO3)2 可减小CrO42—浓度,使平衡左移,溶液由橙色变为黄色,最后为无色,F错误。平衡常数K=9.5×104 可以算出H+浓度是0.1mol/(L,pH= 1;(1)H+(aq)+OH-(aq)=H2O(l); ΔH=" —a" KJ/mol
(2)3Cl2(g)+2Cr3+(aq)+16OH-(aq)=2CrO42-(aq)+6Cl-(aq)+8H2O(l);ΔH="—b" KJ/mol
(3)2CrO42-(aq)+2H+(aq)
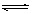 Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol(1) ×16-(2)- (3)得:
Cr2O72-(aq)+H2O(l);ΔH="—c" KJ/mol(1) ×16-(2)- (3)得:Cr2O72- +6Cl-+14H+=3Cl2+2Cr3++7H2O ΔH=(c+b-16a)KJ/mol

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
 [Cu(NH3)3]Ac?CO(aq)(△H<0)
[Cu(NH3)3]Ac?CO(aq)(△H<0)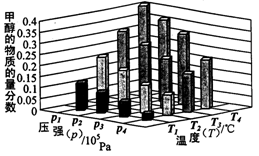


 mol;
mol;

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)

 O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1
O2(g)=ZnO(s) ΔH1=-351.1 kJ·mol-1 3N2+2X+4H2O
3N2+2X+4H2O  .
. 、一283.0 kJ
、一283.0 kJ 、
、 均大于300℃):
均大于300℃):
 时,从反应开始到反应达到平衡,生成甲醇的平均速率为:
时,从反应开始到反应达到平衡,生成甲醇的平均速率为:
 增大
增大