��Ŀ����
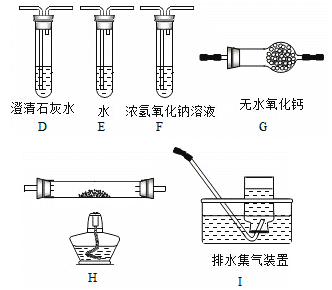
����Ŀ������һ���Ȼ�����Ʒ�к�������̼��ء�����غͲ�����ˮ�����ʡ�Ϊ���ᴿ�Ȼ��أ��Ƚ���Ʒ��������ˮ�У���ֽ������ˣ��ٽ���Һ����ͼ��ʾ������в�����

�ش��������⣺
��1���Լ�I�Ļ�ѧʽΪ_______�������Լ�I�ٶ�Ӧ��ʵ�������______�����з�����Ӧ�����ӷ���ʽΪ________��
��2��������Һ�е� �Ƿ���SO42-�ķ�����______________________________________��
��3���Լ����Ļ�ѧʽΪ_______�����м����Լ�����Ŀ����__________��
��4���Լ�����������________�����з�����Ӧ�����ӷ���ʽΪ_________��
��5��ijͬѧ��ȡ�ᴿ�IJ�Ʒ0.745g���ܽ������100mL����ƿ�У�ȡ25.00mL��Һ����0.1000 mol��L![]() ������������Һ��Ӧ����Ӧ��������������Һ�����Ϊ23.50 mL���ò�Ʒ�Ĵ���Ϊ_________________��
������������Һ��Ӧ����Ӧ��������������Һ�����Ϊ23.50 mL���ò�Ʒ�Ĵ���Ϊ_________________��
���𰸡� BaCl2 ���� Ba2++SO42-=BaSO4 ����Ba2++CO32-=BaCO3�� ȡ������Һ���Թ��У������м���������ᣬ�ټ���BaCl2��Һ�����а�ɫ�������ɣ�����SO42-����֮���� K2CO3 ��ȥ�����Ba2+ ���� CO32-+2H+=CO2��+H2O 94%
����������1��Ҫ��������������������Ӻ�̼������ӣ�Ӧ����������Ȼ�����Һ��̼�������������ɲ�����ˮ�ı��Σ�ͬʱ�����Ȼ��أ��ù��˵ķ������з��룬��Ӧ�����ӷ���ʽΪBa2++SO42-=BaSO4 ����Ba2++CO32-=BaCO3�� ��
��2��������Һ�е� �Ƿ���SO42-�ķ�����ȡ������Һ���Թ��У������м���������ᣬ�ټ���BaCl2��Һ�����а�ɫ�������ɣ�����SO42-����֮���ޡ�
��3�����˺����Ȼ������Ȼ�����ҺA��Ȼ����������̼�����Һ��ȥ��Һ�е��Ȼ��������ˣ��õ��Ȼ��غ�̼��ػ��ҺD��
��4��Ҫ���������̼������ӣ�Ҫ�μ����������ᣬ̼������Ӻ����ᷴӦ���ɶ�����̼��ˮ�����ӷ���ʽΪ��CO32-+2H+=CO2��+H2O��
��5����25mL�Ȼ�����Һ���Ȼ��ص����ʵ���Ϊnmol��
KCl+AgNO3=AgCl+KNO3
1mol 1mol
nmol 0.1000molL-1��0.02350L��n=0.002350mol
100mL��Һ�к����Ȼ��ص����ʵ���=0.002350mol��4=0.0094mol��100mL��Һ�к����Ȼ��ص�����=0.0094mol��74.5g/mol=0.7003g����������=(0.7003g/0.745g)��100%=94%���ʴ�Ϊ��94%��

 ��ʦ������Ԫ��ĩ���100��ϵ�д�
��ʦ������Ԫ��ĩ���100��ϵ�д� ��У������Ԫͬ��ѵ��������ϵ�д�
��У������Ԫͬ��ѵ��������ϵ�д�����Ŀ��Ϊ̽��ͭ��ϡ���ᷴӦ�IJ��PӰ�췴Ӧ���ʵ���Ҫ���أ���������ʵ�顣
ʵ��һ ̽��ͭ��ϡ���ᷴӦ�IJ���ʵ��װ����ͼ��ʾ���������Ѽ�顣

��֪��FeSO4��NO===[Fe(NO)]SO4���÷�Ӧ�ϻ�����������һ����[Fe(NO)]2��ʱͻ������
��ɫ��
(1)ʵ�鿪ʼʱ�Ƚ�Y���Թ���ʢ��̼��Ƶ�֧����б����������ϡ���ᣬ��ʵ�������Ŀ����___________________________________________________________��
(2)ͭƬ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ____________________________________��
(3)��ʵ��A���ɵ������У�����NO2����B��ʵ������Ϊ__________________��
��ֻ��NO���ɣ���B��ʵ��������_________________��
ʵ��� ̽����ѧ��Ӧ����Է�Ӧ���ʵ�Ӱ��
�������ʵ�飬������ͼװ�òⶨ��Һͻ��������ɫ��ʱ�䡣
��� | �¶� | ͭƬ/(g) | ����/mL | ����ͭ/g |
1 | 25 �� | �� | �� | �� |
2 | 25 �� | 5 | 20 | 0.5 |
3 | 25 �� | 5 | 20 | 1.0 |
(4)�뽫�ϱ���ʵ��1��ʵ��������д������
��________����________����________��
(5)ͨ��ʵ�鷢��ʵ��1��2��3�ķ�Ӧ���ʲ������Ա仯��Ϊ�ﵽʵ��Ŀ�Ļ���Ҫ�������е�ʵ����_______________________________________________________��