题目内容
【题目】用98%的浓硫酸(其密度为1.84 g/cm3)配制100 mL 1.0 mol·L-1稀硫酸,
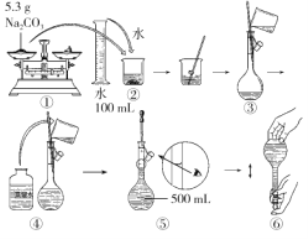
实验步骤如下:① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④检漏、 转移、洗涤 ⑤ 定容、摇匀
若实验仪器有:A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶 E.10 mL量筒 F.胶头滴管 G.50 mL烧杯 H.100 mL容量瓶
回答下列问题:
(1)需量取浓硫酸的体积为__________mL。
(2)实验时选用的仪器有(填序号) _______________,
(3)配制过程中,下列情况会使配制结果偏高的是(填序号) _______________
①定容时仰视刻度线观察液面 ②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,未再加蒸馏水补至刻度线
④.所用的浓硫酸长时间放置在密封不好的容器中⑤用量筒量取浓硫酸时仰视读数
(4)检验试剂瓶中的溶液含有SO42- 的操作是____________________________________
【答案】 5.4 C、E、F、G、H ⑤ 取瓶中少量的溶液于试管中,先加入足量的盐酸,再加入氯化钡溶液有白色沉淀产生,说明含有SO42-
【解析】试题分析:本题考查一定体积物质的量浓度溶液的配制和误差分析,SO42-的检验。
(1)根据稀释前后溶质物质的量不变,1.84g/mLV(浓硫酸)![]() 98%=1mol/L
98%=1mol/L![]() 0.1L
0.1L![]() 98g/mol,V(浓硫酸)=5.4mL。
98g/mol,V(浓硫酸)=5.4mL。
(2)量取5.4mL浓硫酸应选用10mL量筒,配制100mL溶液应选用100mL容量瓶,实验时需要的仪器为:10mL量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,需要的仪器为C、E、F、G、H。
(3)根据cB=![]() 分析。①定容时仰视刻度线观察液面,溶液体积偏大,所配溶液浓度偏低;②容量瓶使用时未干燥,对所配溶液浓度无影响;③定容后经振荡、摇匀、静置,发现液面低于刻度线,未再加蒸馏水补至刻度线,溶质物质的量和溶液体积不变,对所配溶液浓度无影响;④所用的浓硫酸长时间放置在密封不好的容器中,由于浓硫酸具有吸水性,硫酸物质的量偏小,所配溶液浓度偏低;⑤用量筒量取浓硫酸时仰视读数,所量取的浓硫酸的体积偏大,所配溶液浓度偏高;使配制结果偏高的是⑤。
分析。①定容时仰视刻度线观察液面,溶液体积偏大,所配溶液浓度偏低;②容量瓶使用时未干燥,对所配溶液浓度无影响;③定容后经振荡、摇匀、静置,发现液面低于刻度线,未再加蒸馏水补至刻度线,溶质物质的量和溶液体积不变,对所配溶液浓度无影响;④所用的浓硫酸长时间放置在密封不好的容器中,由于浓硫酸具有吸水性,硫酸物质的量偏小,所配溶液浓度偏低;⑤用量筒量取浓硫酸时仰视读数,所量取的浓硫酸的体积偏大,所配溶液浓度偏高;使配制结果偏高的是⑤。
(4)检验试剂瓶中的溶液含有SO42- 的操作是:取试剂瓶中少量的溶液于试管中,先加入足量的盐酸,再加入氯化钡溶液有白色沉淀产生,说明含有SO42-。

 名校课堂系列答案
名校课堂系列答案